
【题目】某化学学习小组在实验室模拟工业法制取Br2,装置如图所示。

(1)仪器M的名称是________。
(2)实验室制取Cl2在通入装置A之前_______(填“需要”或“不需要”)除杂。
(3)实验前检査装置气密性的方法是_______________。
(4)反应过程中Br2在装置B中与Na2CO3反应生成NaBr和NaBrO3。为使装置A中产生的Br2尽可能被吸收,可采取的合理措施是_____________。
(5)反应结束后,取下装置B,向装置B中加入稀H2SO4会生成Br2,该反应的离子方程式为______________。
【答案】
(1)烧杯;
(2)不需要;
(3)关闭K1,打开K2,在烧杯C中加入适量水,将导管末端浸入水中,缓慢鼓动气,观察导管末端有没有气泡产生;
(4)通过气唧,缓慢鼓入空气;
(5)6H++5Br-+BrO3-=3Br2+3H2O;
【解析】
试题分析:(1)根据装置图,仪器M是烧杯,故答案为:烧杯;
(2)实验室制取的Cl2中含有氯化氢和水蒸气,氯化氢和水蒸气对实验无影响,通入装置A之前不需要除去,故答案为:不需要;
(3)实验前检査装置气密性的方法是关闭K1,打开K2,在烧杯C中加入适量水,将导管末端浸入水中,缓慢鼓动气,观察导管末端有没有气泡产生,故答案为:关闭K1,打开K2,在烧杯C中加入适量水,将导管末端浸入水中,缓慢鼓动气,观察导管末端有没有气泡产生;
(4)溴容易挥发,为使装置A中产生的Br2尽可能被吸收,可采取的合理措施是通过气唧,缓慢鼓入空气,故答案为:通过气唧,缓慢鼓入空气;
(5)向装置B中加入稀H2SO4,NaBr和NaBrO3发生氧化还原反应生成Br2,反应的离子方程式为6H+ +5Br- +BrO3-=3Br2+3H2O,故答案为:6H+ +5Br- +BrO3-=3Br2+3H2O。


 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案科目:高中化学 来源: 题型:
【题目】现今太阳能光伏产业蓬勃发展,推动了高纯硅的生产与应用。回答下列问题:
Ⅰ.工业上用“西门子法”以硅石(SiO2)为原料制备冶金级高纯硅的工艺流程如下图所示:

己知:SiHCl3 室温下为易挥发、易水解的无色液体。
(1)“还原”过程需要在高温条件下,该反应的主要还原产物为_____________。
(2)“氧化”过程反应温度为200~300℃,该反应的化学方程式为__________。
(3)“氧化”、“分离”与“热解”的过程均需要在无水、无氧的条件下,原因是_________________。
(4)上述生产工艺中可循环使用的物质是_________、________(填化学式)。
Ⅱ.冶金级高纯硅中常含有微量的杂质元素,比如铁、硼等,需对其进行测定并除杂,以进一步提高硅的纯度。
(5)测定冶金级高纯硅中铁元素含量
将m g 样品用氢氟酸和硝酸溶解处理,配成V mL 溶液,用羟胺(NH2OH,难电离)将Fe3+还原为Fe2+后,加入二氮杂菲,形成红色物质。利用吸光度法测得吸光度A 为0.500(吸光度A与Fe2+浓度对应曲线如图)。

① 酸性条件下,羟胺将Fe3+还原为Fe2+,同时产生一种无污染气体,该反应的离子方程式为__________________________________。
② 样品中铁元素的质量分数表达式为____________________(用字母表示)。
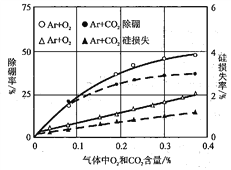
(6)利用氧化挥发法除冶金级高纯硅中的硼元素
采用Ar等离子焰,分别加入O2或CO2,研究硼元素的去除率和硅元素的损失率,实验结果如下图所示。在实际生产过程,应调节O2或CO2的合理比例的原因是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应N2+3H2![]() 2NH3的能量变化如图所示,该反应的热化学方程式是
2NH3的能量变化如图所示,该反应的热化学方程式是

A. N2(g)+3H2(g) ![]() 2NH3(l) △H=2(a-b--c)kJ/mol
2NH3(l) △H=2(a-b--c)kJ/mol
B. N2(g)+3H2(g) ![]() 2NH3(l) △H=2(b-a)kJ/mol
2NH3(l) △H=2(b-a)kJ/mol
C. 1/2 N2(g)+3/2H2(g) ![]() NH3(l) △H=(b+c-a)kJ/mol
NH3(l) △H=(b+c-a)kJ/mol
D. 1/2 N2(g)+3/2H2(g) ![]() NH3(g) △H=(a+b)kJ/mol
NH3(g) △H=(a+b)kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子,能在溶液中大量共存的是
A. Na+ 、Mg2+ 、Cl- 、SO42- B. Na+ 、Ca2+ 、CO32- 、NO3-
C. Na+ 、H+ 、Cl- 、CO32- D. K+ 、Al3+ 、SO42- 、OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸晶体(H2C2O4·xH2O)无色,熔点为101℃,易溶于水,受热易脱水、升华,170℃以上分解,草酸钙难溶于水。某研究性小组按照下图装置,检验草酸晶体的分解产物中含有CO、CO2。已知C、E、H中盛装澄清石灰水,D中盛装浓NaOH溶液,G中盛有CuO。

(1)装置B的主要作用是_______。
(2)装置C中反应的离子方程式为_______。
(3)装置D的作用是_______。
(4)装置F所盛的药品是_______。
(5)能证明草酸晶体分解产物中有CO的现象是_______。
(6)H后连接的尾气处理装置为_______。(从“Ⅰ”“Ⅱ”中选择)
(7)为测定草酸晶体分子式(H2C2O4·xH2O) 中x的值,现做如下实验。
①称取6.3 g草酸晶体,将其配置成100.0 mL水溶液为待测溶液;
②取25.0 mL待测溶液放入锥形瓶中,再加入适量的稀硫酸;
③用浓度为0.4 mol/L的KMnO4标准溶液进行滴定,达到滴定终点时,用去12.50 mL KMnO4溶液。
回答下列问题。
写出H2C2O4和酸性KMnO4溶液反应的化学方程式_______;经计算x=_______。
(8)依据以上实验,写出草酸晶体(H2C2O4·xH2O)受热分解的化学方程式_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.C2H6与C3H8没有同分异构体,CH2O2与C2H4O2属于同系物
B.一定条件下,乙酸乙酯、淀粉、蛋白质、乙烯都能与水发生水解反应
C.一定条件下,完全燃烧14g含氧质量分数为a的乙烯、乙醛混合气体,则生成水的质量为18(1-a)g
D.全降解塑料(![]() )可由单体环氧丙烷(
)可由单体环氧丙烷(![]() )和CO2缩聚制得
)和CO2缩聚制得
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮的化合物应用广泛,但氮氧化物是重要的空气污染物,应降低其排放。
(1)用CO2和NH3可合成氮肥尿素[CO(NH3)2]
已知:①2NH3(g)+CO2(g)=NH2CO2NH4 (s) △H=-159.5 kJ·mol-1
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) △H=+116.5 kJ·mol-1
③H2O(l)=H2O(g) △H=+44 kJ·mol-1
用CO2和NH3合成尿素(副产物是液态水)的热化学方程式为______________。
(2)工业上常用如下反应消除氮氧化物的污染:
CH4(g)+2NO2(g)![]() N2(g)+CO2(g)+2H2O(g) △H
N2(g)+CO2(g)+2H2O(g) △H
在温度为T1和T2时,分别将0.40molCH4和1.0molNO2充入体积为1L的密闭容器中,n(CH4)随反应时间的变化如右图所示:
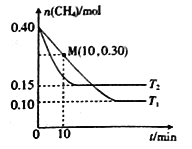
①根据右图判断该反应的△H________0(填“>”、“<”或“=”),理由是______________。
②温度为T1时,0~10min内NO2的平均反应速率v(NO2)=__________,反应的平衡常数K=___(保留三位小数)
③该反应达到平衡后,为在提高反应速率同时提高NO2的转化率,可采取的措施有______(填标号)。
A.改用高效催化剂 B.升高温度
C.缩小容器的体积 D.增加CH4的浓度
(3)利用原电池反应可实现NO2的无害化,总反应为6NO2+8NH3=7N2+12H2O,电解质溶液为NaOH溶液,工作一段时间后,该电池正极区附近溶液pH________(填“增大”、“减小”或“不变”),负极的电极反应式为___________________。
(4)氮的一种氢化物HN3,其水溶液酸性与醋酸相似,则NaN3溶液中各离子浓度由大到小的顺序为________;常温下,将amol·L-1 的HN3与bmol·L-1 的Ba(OH) 2溶液等体积混合,充分反应后,溶液中存在2c(Ba2+)=c(N3-),则该混合物溶液呈_______(填“酸”、“碱”或“中”)性,溶液中c(HN3)=_________ mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃时,H2R及其钠盐的溶液中,H2R、HR-、R2-分别在三者中所占的物质的量分数(α)随溶液pH变化关系如下图所示,下列叙述错误的是

A. H2R是二元弱酸,其Ka1=1×10-2
B. NaHR在溶液中水解程度小于电离程度
C. pH<7.2的溶液中一定存在:c( Na+)>c( HR-) > c(R2- )>c(H+)>c(OH-)
D. 含Na2R与NaHR各0.1 mol的混合溶液的pH=7.2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com