
| 20mL×0.0025mol/L |
| 25mL |
| 5mL×0.01mol/L |
| 25mL |


科目:高中化学 来源: 题型:
| A、向饱和AgCl水溶液中加入盐酸,Ksp值变大 |
| B、用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小 |
| C、在一定温度下AgCl的水溶液中,Ag+和Cl-物质的量浓度的乘积是一个常数 |
| D、沉淀反应中常加过量的沉淀剂,其目的是使沉淀完全 |
查看答案和解析>>
科目:高中化学 来源: 题型:
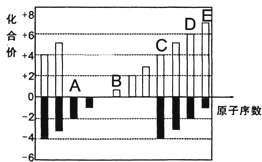 A、B、C、D、E均为短周期元素,其化合价与原子序数的关系如图所示.
A、B、C、D、E均为短周期元素,其化合价与原子序数的关系如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
A、氨气:N2+3H2
| ||||
B、铝:2Al2O3(熔融)
| ||||
C、氯气:MnO2+4HCl(浓)
| ||||
D、硫酸:2SO2+O2
|
查看答案和解析>>
科目:高中化学 来源: 题型:
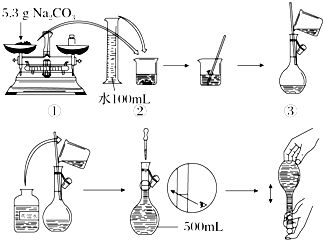 用Na2CO3?10H2O晶体,配制0.2mol?L-1的Na2CO3溶液480mL.
用Na2CO3?10H2O晶体,配制0.2mol?L-1的Na2CO3溶液480mL.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③④⑤ |
| B、④⑤①②③ |
| C、⑤④①②③ |
| D、④⑤①③② |
查看答案和解析>>
科目:高中化学 来源: 题型:
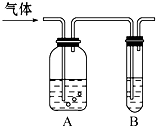 如图把气体缓慢通过盛有足量试剂的试剂瓶A,在试管B中可以观察到明显现象的是( )
如图把气体缓慢通过盛有足量试剂的试剂瓶A,在试管B中可以观察到明显现象的是( ) | 选项 | 气体 | A中试剂 | B中试剂 |
| A | SO2、CO2 | 酸性KMnO4溶液 | 品红溶液 |
| B | Cl2、HCl | 浓硫酸 | KI淀粉溶液 |
| C | NH3、CO2 | 浓硫酸 | 酚酞试液 |
| D | CO2、HCl | 饱和NaHCO3溶液 | AgNO3溶液 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com