
下列说法不正确的是( )
|
| A. | 分子式为C5H10O2的羧酸共有3种 |
|
| B. | 分子式为C3H9N的异构体共有4个 |
|
| C. | 某烷烃CnH2n+2的一个分子中,含有共价键的数目是3n+1 |
|
| D. | 某烷烃CnH2n+2的一个分子中,含有非极性键的数目是n﹣1 |
| 同分异构现象和同分异构体;物质结构中的化学键数目计算.. | |
| 专题: | 化学键与晶体结构;同系物和同分异构体. |
| 分析: | A.C5H10O2属于羧酸的同分异构体为丁烷中的1个H原子被﹣COOH夺取,即由丁基与﹣COOH构成,其同分异构体数目与丁基异构数目相等; B.根据氮原子可以形成取代基,也可形成主链; C.烷烃中只含有C﹣C和C﹣H键,设烷烃的分子式为CnH2n+2,则含有的C﹣C键数目为n﹣1,C﹣H键数目为2n+2; D.烷烃中只含有C﹣C和C﹣H键,设烷烃的分子式为CnH2n+2,则含有的C﹣C共价键(非极性键)数目为n﹣1,C﹣H数目为2n+2(极性键); |
| 解答: | 解:A.C5H10O2属于羧酸的同分异构体为丁烷中的1个H原子被﹣COOH夺取,即由丁基与﹣COOH构成,其同分异构体数目与丁基异构数目相等,已知丁基共有4种,可推断分子式为C5H10O2属于羧酸的同分异构体数目也有4种,故A错误; B.分子式为C3H9N的异构体有:CH3CH2CH2NH2,CH3CHNH2CH3,CH3CH2NHCH3,N(CH3)3,共4种,故B正确; C.某烷烃CnH2n+2的一个分子中,含有的C﹣C键数目为n﹣1,C﹣H键数目为2n+2,共含有共价键的数目是3n+1,故C正确; D.某烷烃CnH2n+2的一个分子中,含有非极性键即C﹣C键的数目是n﹣1,故D正确; 故选:A; |
| 点评: | 本题主要考查了同分异构体的书写、分子中共价键的数目的计算,注意同种元素之间形成非极性共价键,不同元素之间形成极性共价键. |


科目:高中化学 来源: 题型:
乙烯是重要化工原料,其产量是一个国家石油化工发展水平的标志。请回答:
(1)在一定条件下,乙烷和乙烯都能制备氯乙烷(C2H5Cl)。
①用乙烷制备氯乙烷的化学方程式是___________________________________________
________________,该反应的类型是________。
②用乙烯制备氯乙烷的化学方程式是__________________________________________
________________,该反应的类型是________。
比较上述两种方法,第________种方法更好。其原因是
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
(2)此外,乙烯大量用来生产环氧乙烷,生产工艺主要有两种

根据绿色化学的原则,理想的生产工艺是原子经济性好的反应,工艺一的原子利用率________100%(填“<”、“=”、“>”,下同);工艺二的利用率为________100%,因此,在实际生产中,采用工艺________更环保,更经济。
查看答案和解析>>
科目:高中化学 来源: 题型:
某氯原子的质量是a g,12C原子的质量是b g,用NA表示阿伏加德罗常数,下列说法中正确的是( )
①氯元素的相对原子质量一定是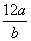 ②m g该氯原子的物质的量一定是
②m g该氯原子的物质的量一定是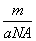 mol ③该氯原子的摩尔质量是aNA g/mol ④a g该氯原子所含质子数是17 mol
mol ③该氯原子的摩尔质量是aNA g/mol ④a g该氯原子所含质子数是17 mol
A.①③ B.②④
C.①④ D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)甲烷的分子个数为1.204×1023,则甲烷的物质的量为 mol,所含的原子个数共有 个,与这些甲烷质量相等的O2的物质的量为 mol。
(2)含有相同氧原子数目的NO和CO2两种气体,其质量比 ,物质的量比为 ,在标准状态下,体积比为 。
(3)一定量的氢气在氯气中燃烧,所得混合物用100 mL 3.00 mol/L的NaOH溶液(密度为1.12g/mL)恰好完全吸收,测得溶液中含有NaClO的物质的量为0.05mol。
①原NaOH溶液的质量分数为 。
②所得溶液中Cl-的物质的量为 mol。
③所用氯气和参加反应的氢气的物质的量之比n(Cl2)∶n(H2)= 。
查看答案和解析>>
科目:高中化学 来源: 题型:
如图是某同学设计的原电池装置,下列叙述中正确的是( )

|
| A. | 电极Ⅰ上发生还原反应,作原电池的负极 |
|
| B. | 电极Ⅱ的电极反应式为:Cu2++2e﹣=Cu |
|
| C. | 该原电池的总反应为:2Fe3++Cu=Cu2++2Fe2+ |
|
| D. | 盐桥中装有含氯化钾的琼脂,其作用是传递电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E、F、G都是链状有机物,它们的转化关系如图所示.A只含一种官能团,D的相对分子质量与E相差42,D的核磁共振氢谱图上有3个峰,且峰面积之比为1:3:6,请回答下列问题:
已知:Mr(R﹣Cl)﹣Mr(ROH)=18.5,Mr(RCH2OH)﹣Mr(RCHO)=2,Mr表示相对分子质量.
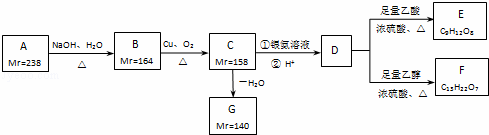
(1)A中含有的官能团是 .
(2)写出D的分子式 .
(3)下列有关A~G的说法正确的是 .
a.每个A分子中含有官能团的数目为4个
b.B中所有官能团均发生反应生成C
c.C生成G只有1种产物
d.G存在顺反异构现象
(4)写出B生成C的化学方程式 .
(5)芳香族化合物H与G互为同分异构体,1mol H与足量氢氧化钠溶液反应消耗2mol NaOH,且H苯环上的一氯代物只有两种,写出其中任意一个符合条件的H的结构简式 或 .
(6)E与足量NaOH溶液共热,此反应的化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下述实验方案能达到实验目的的是
| 编号 | A | B | C | D |
| 实验 方案 |
|
|
|
|
| 实验 目的 | 实验室制备乙酸乙酯 | 分离乙酸和水 | 验证溴乙烷在氢氧化钠乙醇溶液中发生消去反应产生的乙烯 | 收集乙烯并验证它与溴水发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.常温下,将pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均降低
B.温度一定时,向水中滴加少量酸或碱形成稀溶液,水的离子积常数Kw不变
C.8NH3(g)+6NO2(g)=7N2(g)+12H2O(g) H<0,则该反应一定不能自发进行
D.由于Ksp(BaSO4)<Ksp(BaCO3),因此不可能使BaSO4沉淀转化为BaCO3沉淀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com