
常温下,向10 mL 0.1 mol·L-1的H2C2O4溶液中逐滴加入0.1 mol·L-1 KOH溶液,所得滴定曲线如图所示。下列说法正确的是
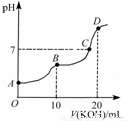
A.KHC2O4溶液呈弱碱性
B.B点时:c(HC2O4-)>c(K+)>c(H+)>c(OH-)
C.C点时:c(HC2O4-)+c(C2O42-)+c(H2C2O4)<c(K+)<c(HC2O4-)+2c(C2O42-)+c(H2C2O4)
D.D点时:c(H+)+c(HC2O4-)+c(H2C2O4)=c(OH-)
科目:高中化学 来源:2015-2016学年山东省高二上学期期中测试化学试卷(解析版) 题型:选择题
下列操作中正确的是
A.用试管取出试剂瓶中Na2CO3溶液,发现取量过多,又把过量的试剂倒入试剂瓶中
B.过滤时,漏斗下端紧贴烧杯内壁
C.加热试管内物质时,试管底部与酒精灯灯芯接触
D.向试管中滴加液体时,胶头滴管紧贴试管内壁
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省高一上学期期中测试化学试卷(解析版) 题型:填空题
(8分)一份无色溶液中可能含有Na+ 、Fe3+、H+ 、Mg2+、CO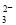 、OH-、HCO
、OH-、HCO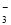 、
、
Cl-、SO42-等离子中的若干种。为了确定溶液的组成,进行了如下操作:
①向溶液中滴加酚酞试液,溶液显红色;
②取2 mL溶液,先加足量稀硝酸酸化,有气体产生,再加氯化钡溶液进行检验,没有明显现象;
(1)原溶液中一定存在的离子是 ,一定不存在的离子是 。
(2)经过上述操作后,还不能肯定是否存在的离子是 。对可能含有的离子,如何进行实验以进一步检验。 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省高一上学期期中测试化学试卷(解析版) 题型:填空题
碘是人体不可缺乏的元素,为了防止碘缺乏,现在市场上流行一种加碘盐,就是在精盐中添加一定量的KIO3进去。某研究小组为了检测某加碘盐中是否含有碘,查阅了有关的资料,发现其检测原理是:KIO3+5KI+3H2SO4=3I2+3H2O+3K2SO4
(1)该反应氧化产物与还原产物质量比是_________________;
(2)先取少量的加碘盐加蒸馏水溶解,然后加入稀硫酸和KI溶液,最后加入一定量的CCl4,振荡,这时候,观察到的现象是_________________;
(3)某学生在一次分液操作中发现上下层溶液都是无色液体,无法知道分液漏斗中的液体哪一层是有机层,哪一层是水层,请你用简单的方法帮他鉴别出来,写出有关步骤及判断方法___________________。
(4)在容量瓶的使用方法中,下列操作正确的是____________
A.使用容量瓶前检验是否漏水
B.容量瓶用水洗净后,再用待配溶液洗涤
C.配制溶液时,若试样是液体,用量筒取样后用玻璃棒引流倒入容量瓶中,缓慢加水至刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线
D.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀
(5)上面实验中用到一定物质的量浓度的稀硫酸,若配制0.5mol/L的硫酸溶液450mL,需用量筒量取质量分数为98%、密度为1.84g/cm3的浓硫酸的体积为_________mL,如果实验室有15mL、20mL、50mL量筒,应选用___________mL量筒最好。
(6)下面操作造成所配稀硫酸溶液浓度偏高的是__________
A.溶解的时候溶液没有冷却到室温就转移
B.转移时没有洗涤烧杯、玻璃棒
C.向容量瓶加水定容时眼睛俯视液面
D.用量筒量取浓硫酸后洗涤量筒并把洗涤液转移到容量瓶
E.摇匀后发现液面低于刻度线,又加蒸馏水至刻度线
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省淄博市高二上学期期中测试化学试卷(解析版) 题型:填空题
(1)已知1g碳粉在氧气中完全燃烧放出的热量是32.8 kJ,试写出表示碳燃烧热的热化学方程式
(2)运用化学反应原理研究氮、氧等单质及其化合物的反应有重要意义。
①合成氨反应N2(g)+3H2(g) 2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,平衡 移动(填“正向”、“逆向”或“不”);使用催化剂反应的△H (填“增大”、“减小”或“不改变”)。
2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,平衡 移动(填“正向”、“逆向”或“不”);使用催化剂反应的△H (填“增大”、“减小”或“不改变”)。
②已知:O2(g)  O2+(g)+e- △H1=+1175.7 kJ·mol—1
O2+(g)+e- △H1=+1175.7 kJ·mol—1
PtF6(g)+e- PtF6-(g) △H2=-771.1 kJ·mol—1
PtF6-(g) △H2=-771.1 kJ·mol—1
O2PtF6(s) O2+(g)+PtF6-(g) △H3=+482.2 kJ·mol—1
O2+(g)+PtF6-(g) △H3=+482.2 kJ·mol—1
则反应O2(g)+PtF6(g)  O2PtF6 (s)的 △H=_____________
O2PtF6 (s)的 △H=_____________
查看答案和解析>>
科目:高中化学 来源:2016届湖南省高三上学期第三次月考化学试卷(解析版) 题型:实验题
某课外活动小组欲对铝镁合金进行研究,测定其中镁的质量分数,他们利用盐酸、氢氧化钠溶液设计了三种不同的实验方案:
方案一:铝镁合金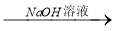 测定生成气体的体积
测定生成气体的体积
方案二:铝镁合金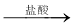 测定生成气体的体积
测定生成气体的体积
方案三:铝镁合金 溶液
溶液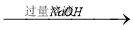
 称量灼烧产物的质量。
称量灼烧产物的质量。
(1)写出方案一中发生反应的离子方程式 。
(2)实验小组根据方案=设计了两个实验装置,如下圈(图中的铁架台已省略)。
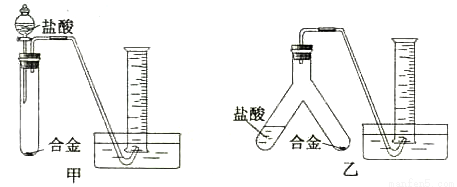
你认为选择 (选填甲或乙)装置进行实验更合理,误差更小。
(3)用方案三进行实验时,除了称量灼烧产物质量外,还需称量的是 。
(4)拓展研究:在向铝镁合金溶于盐酸后的溶液中加入过量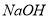 溶液时,生成沉淀的质量与加入
溶液时,生成沉淀的质量与加入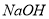 溶液体积的关系可用数轴关系表示:
溶液体积的关系可用数轴关系表示:
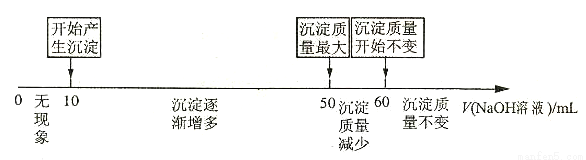
请你判断,根据上图数轴申的数据能否求出合金中镁的质量分数? _______(选填“能”或“不能”)
下列①②两题选一题作答。
①若不能求出合金中镁的质量分数,请说明理由 。
②若能求出合金中镁的质量分数,则镁的质量分数为 。
查看答案和解析>>
科目:高中化学 来源:2016届湖南省高三上学期第三次月考化学试卷(解析版) 题型:选择题
下列化学用语表示正确的是
A.NaH与重水反应的方程式:NaH+D2O===NaOH+D2↑
B.三氟化氮的电子式: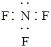
C.熔融状态下硫酸氢钠的电离方程式:NaHSO4(熔融)===Na++HSO4-
D.硫化钠溶液显碱性的原因:S2-+H2O  H2S + 2OH-
H2S + 2OH-
查看答案和解析>>
科目:高中化学 来源:2016届湖北省襄阳市高三上学期期中测试化学试卷(解析版) 题型:填空题
如图是可用于测量阿伏加德罗常数的装置示意图,其中A是纯铜片、B是石墨,插在100mLCuSO4稀溶液中,铜片、石墨与引出导线相连,引出端分别为X、Y。
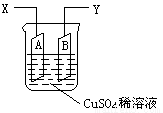
(1)当以IA的电流电解6min后,测得铜片A质量减少2.56g,则图装置中的X端应与直流电的 极相连。
(2)电解后将电源反接,2IA的电流电解6min后,假设溶液体积不变,测得溶液中CuSO4物质的量浓度为0.1mol/L,则原溶液中CuSO4物质的量浓度 mol/L。溶液中H+的物质的量浓度为 mol/L。
(3)列式计算实验测得的阿伏加德罗常数NA(用I表示) mol-1。(已知电子电量e=1.60×10–19C)
查看答案和解析>>
科目:高中化学 来源:2016届江西省高安市高三上学期第二次段考化学试卷(解析版) 题型:选择题
25℃时,下列各组离子在指定溶液中可能大量共存的是
A.无色溶液中: Al3+、NH4+、Cl-、S2-
B.由水电离得到的c(H+)=1×10-13mol·L-1的溶液中:Mg2+、Cu2+、SO42-、NO3-
C.0. 1 mol·L-1 NH4HCO3溶液中: K+、Na+、AlO2-、Cl-
D.中性溶液中可能大量存在Fe3+、K+、Cl-、SO42-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com