
实验欲配制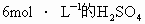 溶液.现有三种有同浓度的硫酸:①
溶液.现有三种有同浓度的硫酸:①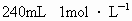 的硫酸;②150mL25%的硫酸
的硫酸;②150mL25%的硫酸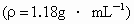 ;③足量
;③足量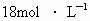 的浓
的浓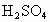 .现有三种规格容量瓶:250mL、500mL、1000mL.配制要求:①、②两种硫酸全部用完,不足部分由③补充.问需要多少毫升浓
.现有三种规格容量瓶:250mL、500mL、1000mL.配制要求:①、②两种硫酸全部用完,不足部分由③补充.问需要多少毫升浓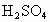 ?
?
|
解:依题意关键是确定配制  硫酸溶液的体积,其体积只有三个数值可选择:250mL、500mL、1000mL,计算时只要在欲配制的体积范围内,各种浓度硫酸混合不必考虑体积变化. 硫酸溶液的体积,其体积只有三个数值可选择:250mL、500mL、1000mL,计算时只要在欲配制的体积范围内,各种浓度硫酸混合不必考虑体积变化.
首先求出②的硫酸溶液的物质的量浓度,然后依据所配制的溶液中溶质的物质的量等于所需三种硫酸溶液中溶质的物质的量之和即可求出浓  的体积. 的体积. 溶液物质的量浓度: 溶液物质的量浓度:
确定配制  硫酸溶液的体积; 硫酸溶液的体积;
因为①、②两溶液体积和约为 240mL+150mL=390mL,而它们的浓度又都小于 ,所以不能选用250mL容量瓶. ,所以不能选用250mL容量瓶.
设配制 500mL,所需浓 体积为x, 体积为x,
因为 128.3+240+150>500,所以500mL容量瓶也不能选用.设酸制1000mL,需浓 体积为y. 体积为y.
答:需要 295mL浓硫酸. |


 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源: 题型:058
实验欲配制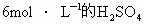 溶液.现有三种有同浓度的硫酸:①
溶液.现有三种有同浓度的硫酸:①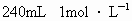 的硫酸;②150mL25%的硫酸
的硫酸;②150mL25%的硫酸 ;③足量
;③足量 的浓
的浓 .现有三种规格容量瓶:250mL、500mL、1000mL.配制要求:①、②两种硫酸全部用完,不足部分由③补充.问需要多少毫升浓
.现有三种规格容量瓶:250mL、500mL、1000mL.配制要求:①、②两种硫酸全部用完,不足部分由③补充.问需要多少毫升浓 ?
?
查看答案和解析>>
科目:高中化学 来源:教材完全解读 苏教版课标版 高中化学 必修1 苏教版课标版 题型:038
实验欲配制6 mol·L-1的H2SO4溶液.现有三种不同浓度的硫酸:①240 mL 1 mol·L-1的硫酸;②150 mL 25%的硫酸(ρ=1.18 g·mL-1);③足量的18 mol·L-1的浓H2SO4.现有三种规格容量瓶:250 mL、500 mL、1000 mL.配制要求:①、②两种硫酸全部用完,不足部分由③补充.问需要多少毫升浓H2SO4?
查看答案和解析>>
科目:高中化学 来源: 题型:
实验欲配制6.00 mol/L的H2SO4溶液.现有三种不同浓度的硫酸:①240 mL 1.00 mol/L的硫酸;②150 mL 25.0%的硫酸(ρ=1.18 g/mL);③足量的18.00 mol/L的浓H2SO4.现有三种规格容量瓶:250 mL、500 mL、1000 mL.配制要求:①、②两种硫酸全部用完,不足部分由③补充.试回答:
(1)选用容量瓶的规格是 。
(2)需要18.0 mol·L-1 H2SO4(aq)的体积是 。
查看答案和解析>>
科目:高中化学 来源:09-10学年宜城市一中高一下学期第一次月考化学卷 题型:实验题
Ⅰ(5分)⑴用14.2g无水硫酸钠配制成500 ml溶液,其物质的量浓度为 ▲ mol/L。
⑵若从上述溶液中取出10 ml,则这10 ml 溶液的物质的量浓度为 ▲ mol/L,含溶质的质量为 ▲ g。
⑶若将上述10 ml 溶液用水稀释到100 ml,所得溶液中Na+的物质的量浓度为 ▲ mol/L;若将稀释后溶液中的SO42-全部沉淀下来,至少需要加入0.1 mol/L的BaCL2溶液
▲ ml 。
Ⅱ(6分)现有36%的醋酸(CH3COOH),密度为1.04g/ml.,
欲配制0.1 mol/L的醋酸250 ml,需要取用36%的醋酸 ▲ ml。
需要使用的实验仪器有烧杯、 ▲ 、 ▲ 、 ▲ 、 ▲ ,
若配制时仅有其中一步操作(如图所示)有错误,其他操作全部正确,则所配醋酸的浓度 ▲ (填“正确”、“偏大”或“偏小”)。
▲ (填“正确”、“偏大”或“偏小”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com