
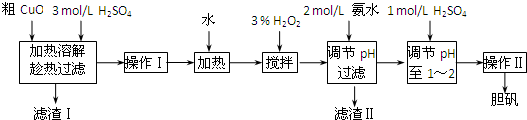
粗CuO是将工业废铜、废铜合金等高温焙烧而成的,杂质主要是铁的氧化物及泥沙。以粗CuO为原料制备胆矾的主要流程如下:

经操作I得到粗胆矾,操作III得到精制胆矾。两步操作相同,具体包括蒸发浓缩、冷却结晶、过滤、洗涤、干燥等步骤。
已知: 、
、 、
、 转化为相应氢氧化物时,开始沉淀和沉淀完全时的pH如下表:
转化为相应氢氧化物时,开始沉淀和沉淀完全时的pH如下表:
|
|
|
|
|
|
开始沉淀时的pH |
2.7 |
7.6 |
5.2 |
|
完全沉淀时的pH |
3.7 |
9.6 |
6.4 |
(1)溶解、过滤需要用到玻璃棒,它的作用是 。
(2)写出加入3% H2O2后发生反应的离子方程式 。(原溶液显酸性)。
(3)加稀氨水调节pH应调至范围 。下列物质可用来替代稀氨水的是 。(填字母)
A.NaOH B.Cu(OH)2 C.CuO D.NaHCO3
(4)操作III析出胆矾晶体后,溶液中还可能存在的溶质为CuSO4、H2SO4、________________。
(5)某学生用操作III所得胆矾进行“硫酸铜晶体结晶水含量”的测定,数据记录如下表所示:
|
|
第一次实验 |
第二次实验 |
|
坩埚质量(g) |
14.520 |
14.670 |
|
坩埚质量 |
17.020 |
18.350 |
|
第一次加热、冷却、称量(g) |
16.070 |
16.989 |
|
第二次加热、冷却、称量(g) |
16.070 |
16.988 |
两次都无须再做第三次加热、冷却、称量,理由是 ,该生此次实验的相对误差为 %(保留1位小数),产生实验误差的原因可能是
(填字母)。
A.加热前称量时坩埚未完全干燥 B.该胆矾中含有受热不分解的杂质
C.加热后坩埚放在干燥器中冷却 D.玻璃棒上沾有的固体未刮入坩埚
(1)搅拌、引流 (1分)
(2)2Fe2+ +H2O2 +2H+ →2Fe3+ +2H2O (2分)
(3)3.7~5.2 (1分) ; BC(2分)
(4)(NH4)2SO4 或NH4HSO4 (1分,写到一个即给分)
(5)已达恒重 (1分);+4.2% (2分);AD (2分)
【解析】
试题分析:(1)溶解、过滤需要用到玻璃棒,它的作用是搅拌、引流。
(2)由于双氧水不稳定,加热易分解生成氧气和水。由于在加入双氧水之前溶液的温度较高,所以加入3% H2O2之前必须进行冷却操作。由于亚铁离子沉淀的pH较大,所以必须将其氧化成铁离子沉淀,因此加入双氧水的目的是氧化亚铁离子,反应的离子方程式为2Fe2+ + H2O2 + 2H+ = 2Fe3+ +2H2O。
(3)要得到胆矾,就必须除去溶液中的铁离子,则根据沉淀时的pH值可知,调节溶液pH的目的是使Fe3+完全转变成Fe(OH)3沉淀;铁离子完全沉淀时的pH=3.7,而铜离子开始沉淀时的pH=5.2,所以溶液的pH应调节到3.7~5.2之间。由于在调节pH的同时,不能引入杂质,因此应该选择氧化铜,Cu(OH)2 来调节溶液的pH。
(4)操作III析出胆矾晶体后,溶液中还可能存在的溶质为CuSO4、H2SO4、(NH4)2SO4 或NH4HSO4。
(5)根据表中的数据两次实验都已达恒重故没必要再进行第三称量。坩埚质量(g)(14.52+14.67)/2= 14.595 实验1:晶体质量:17.02-14.595=2.425水的质量:17.02-16.07=0.95,水的质量分数:0.95/2.425=0.3917,实验2:晶体质量:18.35-14.595=3.755水的质量:18.35-16.99=1.36,水的质量分数:1.36/3.755=0.3622,两次平均水的质量分数:0.3769,五水硫酸铜中水的理论质量数:0.36,相对误差(0.3769-0.360/0.36=0.042。产生实验误差是偏大,即水的质量较多或剩余固体的质量较少,其原因可能是A.加热前称量时坩埚未完全干燥有了多余的水,正确。B.该胆矾中含有受热不分解的杂质会使结果偏低。C.加热后坩埚放在干燥器中冷却,不会带来误差。D.玻璃棒上沾有的固体未刮入坩埚,有一部分固体没有得到称量,相当于剩余的固体质量减小,正确。
考点:考查胆矾制备实验设计与探究以及实验相对误差的分析处理等


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:
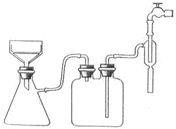
| Fe3+ | Fe2+ | Cu2+ | |
| 氢氧化物开始沉淀时的pH | 1.9 | 7.0 | 4.7 |
| 氢氧化物沉淀完全时的pH | 3.2 | 9.0 | 6.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
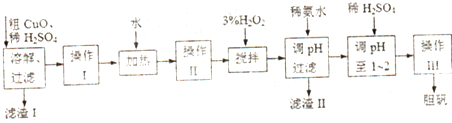
| Fe3+ | Fe2+ | Cu2+ | |
| 开始沉淀的pH | 2.7 | 7.6 | 5.2 |
| 沉淀完全的pH | 3.7 | 9.6 | 6.4 |
查看答案和解析>>
科目:高中化学 来源:2014届江苏省无锡市高三上学期期中调研考试化学试卷(解析版) 题型:实验题
粗CuO是将工业废铜、废铜合金等高温焙烧而成的,杂质主要是铁的氧化物及泥沙。以粗CuO为原料制备胆矾的主要流程如下:
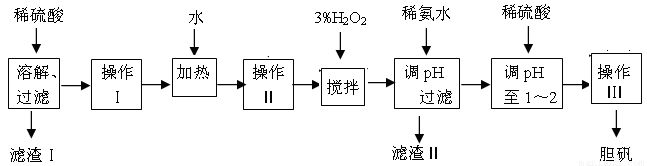
已知Fe3+、Fe2+ 、Cu2+转化为相应氢氧化物时,开始沉淀和沉淀完全时的pH如下表:
|
|
Fe3+ |
Fe2+ |
Cu2+ |
|
开始沉淀时的pH |
2.7 |
7.6 |
5.2 |
|
完全沉淀时的pH |
3.7 |
9.6 |
6.4 |
(1)加入3% H2O2之前必须进行操作Ⅱ,操作Ⅱ的名称是 ;
H2O2参加反应的离子方程式为 。
(2)加稀氨水调节pH的目的是 ,pH应调至 范围。下列物质可用来替代稀氨水的是 。
①NaOH ②Fe2O3 ③CuO ④Na2CO3
(3)经操作Ⅰ得到粗胆矾,操作Ⅲ得到精致胆矾。两步操作相同,具体包括 、 、
过滤、 、干燥等步骤。
查看答案和解析>>
科目:高中化学 来源: 题型:
粗CuO是将工业废铜、废铜合金等高温焙烧而成的,杂质主要是铁的氧化物及泥沙。以粗CuO为原料制备胆矾的主要流程如下:
粗CuO、
稀硫酸 水 3%H2O2 稀氨水 稀硫酸
![]()
![]()
![]()
![]()
![]()
![]()
![]() 溶解、 操作 加热 操作 搅拌 调pH 调pH 操作
溶解、 操作 加热 操作 搅拌 调pH 调pH 操作
![]()
![]()
![]()
![]()
![]()
![]() 过滤 Ⅰ Ⅱ 过滤 至1~2 Ⅲ
过滤 Ⅰ Ⅱ 过滤 至1~2 Ⅲ
滤渣Ⅰ 滤渣Ⅱ 胆矾
已知Fe3+、Fe2+ 、Cu2+转化为相应氢氧化物时,开始沉淀和沉淀完全时的pH如下表:
| Fe3+ | Fe2+ | Cu2+ | |
| 开始沉淀时的pH | 2.7 | 7.6 | 5.2 |
| 完全沉淀时的pH | 3.7 | 9.6 | 6.4 |
(1)加入3% H2O2之前必须进行操作Ⅱ,操作Ⅱ的名称是 ;
H2O2参加反应的离子方程式为 。
(2)加稀氨水调节pH的目的是 ,pH应调至 范围。
下列物质可用来替代稀氨水的是
①NaOH ②Fe2O3 ③CuO ④Na2CO3
(3)经操作Ⅰ得到粗胆矾,操作Ⅲ得到精致胆矾。两步操作相同,具体包括 、 、过滤、 、干燥等步骤。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com