
下列图像所表示的化学知识正确的是
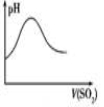
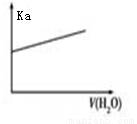
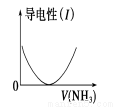
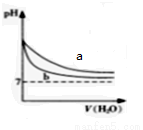
图1 图2 图3 图4
A.图1 SO2气体通入氯水中,溶液pH的变化
B.图2 常温下,向醋酸溶液中加水稀释,Ka的变化
C.图3 向乙酸溶液中通入NH3过程中溶液导电性的变化
D.图4 pH相同的NaOH溶液与氨水稀释过程的pH变化,其中曲线a对应氨水
科目:高中化学 来源:2016-2017学年浙江省高二上期中化学卷(解析版) 题型:选择题
下列说法正确的是
A.任何酸与碱发生中和反应生成1molH2O的过程中,能量变化均相同
B.中和热的实验过程中,环形玻璃搅拌棒材料若用铜代替,则测量出的中和热数值偏小
C.若①2H2(g)+O2(g)=2H2O(g)△H=-akJ·mol-1,
②2H2(g)+O2(g)=2H2O(l)△H=-bkJ·mol-1,则a>b
D.能自发进行的反应一定是放热反应,不能自发进行的反应一定是吸热反应
查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上月考四化学试卷(解析版) 题型:选择题
短周期元素W、X、Y、Z的原子序数依次增加。m、p、r是由这些元素组成的二元化合物。n是元素Z的单质。通常为黄绿色气体,q的水溶液具有漂白性。0.01mol/L r溶液的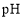 为2,p是甲烷。上述物质的转化关系如图所示。下列说法正确的是
为2,p是甲烷。上述物质的转化关系如图所示。下列说法正确的是
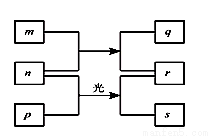
A.原子半径的大小W<X<Y
B.元素的非金属性Z>X>Y
C.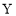 的氢化物常温常压下为气态
的氢化物常温常压下为气态
D.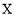 的最高价氧化物对应的水化物为弱酸
的最高价氧化物对应的水化物为弱酸
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省高三上模拟一化学试卷(解析版) 题型:实验题
为研究铜与浓硫酸的反应,某化学兴趣小组进行如下实验。实验装置如图所示:(固定装置已略去)

(1)A中反应的化学方程式为 。
(2)F烧杯中的溶液通常是  。
。
(3)实验过程中,能证明浓硫酸中硫元素的氧化性强于氢元素的现象是 。
(4)实验结束后,证明A装置试管中反应所得产物是否含有铜离子的操作方法是 。
(5)为说明浓硫酸中的水是否影响B装置现象的判断,还须进行一次实验。实验方案为 。
(6)将57.6g的Cu片加入50mL 18 mol/L的H2SO4溶液中并加热,被还原的H2SO4的物质的量为_________
A.小于0.45 mol
B.等于0.45 mol
C.在0.45 mol和0.90 mol之间
D.等于0.90 mol
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省高三上模拟一化学试卷(解析版) 题型:选择题
原子序数依次增大的W、X、Y、Z四种短周期主族元素,W-与氦原子电子层结构相同,W与X原子核外最外层电子数之和与Y原子核外最外层电子数相等,X、Y处于同一周期,Y是地壳中含量最多的元素,Z原子次外层电子数是最外层电子数的4倍。下列说法正确的是
A. 简单离子的半径:X>Y>Z>W
B. 由W、X、Y三种元素组成的化合物水溶液一定显酸性
C. 由X、Y、Z三种元素形成的化合物可能属于共价化合物
D. 由W与Y两种元素形成的化合物中一定只含有极性共价键
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省高三上模拟一化学试卷(解析版) 题型:选择题
汽车尾气中CO、NO2气体在一定条件下可以发生反应:4CO(g)+2NO2(g) 4CO2(g)+N2(g) ΔH=-1200 kJ·mol-1,温度不同(T2>T1)、其他条件相同时,下列图像正确的是
4CO2(g)+N2(g) ΔH=-1200 kJ·mol-1,温度不同(T2>T1)、其他条件相同时,下列图像正确的是

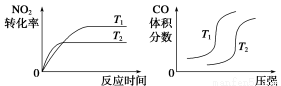

A B C D
查看答案和解析>>
科目:高中化学 来源:2017届江西师大附中高三上学期期中化学试卷(解析版) 题型:填空题
(Ι)HNO2是一种弱酸,且不稳定,易分解生成NO和NO2;它能被常见的强氧化剂氧化;在酸性溶液中它也是一种氧化剂,如能把Fe2+氧化成F e3+。AgNO2是一种难溶于水、易溶于酸的化合物。试回答下列问题:
e3+。AgNO2是一种难溶于水、易溶于酸的化合物。试回答下列问题:
(1)下列方法中,不能用来区分NaNO2和NaCl的是________(填序号)。
A.测定这两种溶液的pH
B.分别在两种溶液中滴加甲基橙
C.在酸性条件下加入KI—淀粉溶液来区别
D.用AgNO3和HNO3两种试剂来区别
(2)某同学把新制的氯水加到NaNO2溶液中,请写出反应的离子方程式:________________。
(3)铝能溶解在碱性亚硝酸盐溶液中,生成能使湿润的红色石蕊变蓝的气体,请写出反应的离子方程式__________________;
(Ⅱ)某暗紫色化合物A在常温和干燥的条件下,可以稳定存在,但它在水溶液中不稳定,一段时间后转化为红褐色沉淀,同时产生一种气体单质。为探究其成分,某学习兴趣小组的同学取化合物A粉末进行试验。经组成分析,该粉末仅含有O、K、Fe三种元素。另取3.96g化合物A的粉末溶于水,滴加足量稀硫酸,向反应后的溶液中加入含有0.08mol KOH的溶液,恰好完全反应。过滤,将洗涤后的沉淀充分灼烧,得到红棕色固体粉末1.60g;将所得滤液在一定条件下蒸发可得到一种纯净的不含结晶水的盐10.44g。
(1)目前,人们针对化合物A的稳定性进行了大量的探索,并取得了一定的进展。
下列物质中有可能提高化合物A水溶液稳定性的是 。
A.醋酸钠 B.醋酸 C.Fe(NO3)3 D.KOH
(2)请设计一个实验方案,研究温度对化合物A溶液稳定性的影响
(3)下图表示足量 Fe粉还原KNO3溶液过程中,测出的溶液中相关离子浓度、pH随时间的变化关系(部分副反应产物曲线略去)。请根据图中信息写出t1时刻前该反应的离子方程式:
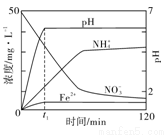
查看答案和解析>>
科目:高中化学 来源:2017届江西师大附中高三上学期期中化学试卷(解析版) 题型:选择题
类比推理是化学中常用的思维方法。下列推理正确的是( )

A.HCl可以用如图装置完成喷泉实验, 推测HF可以用此装置完成喷泉实验
B.Fe与Cl2反应生成FeCl3,推测Fe与I2反应生成FeI3
C.SiH4的沸点高于CH4,推测H2Se的沸点高于H2S
D.NaCl与浓H2SO4加热可制HCl,推测NaBr与浓H2SO4加热可制HBr
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省娄底市等五校高二上期中化学卷(解析版) 题型:选择题
原电池的电极名称不仅与电极材料的性质有关,也与电解质溶液有关。下列说法中不正确的是
A.由Al、Cu、稀H2SO4组成原电池,其负极反应式为:Al-3e-=Al3
B.由Mg、Al、N aOH溶液组成原电池,其负极反应式为:
aOH溶液组成原电池,其负极反应式为:
Al-3e-+4OH-=AlO2-+2H2O
C.由Fe、Cu、FeCl3溶液组成原电池,其负极反应式为:Cu-2e-=Cu2+
D.由Al、Cu、浓硝酸组成原电池,其负极反应式为:Cu-2e-=Cu2+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com