
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源: 题型:阅读理解

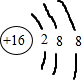
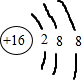
| ||
| △ |
| ||
| △ |
| T/K | 303 | 313 | 323 |
| CA2生成量/(10-1mol) | 4.3 | 5.9 | 6.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:新课程模块教与练·高中化学必修2(苏教版) 苏教版 题型:022
A、B、C、D、E五种主族元素所处周期表的位置如图所示.

已知B元素能与氧元素形成化合物AO2,AO2中氧的质量分数为50%,且A原子中质子数等于中子数,则A元素的原子序数为________,位于第________周期、第________族,A的氧化物除了AO2外还有________;D元素的符号是________,位于________周期、第________族;B与氢气反应的化学反应方程式为________;E单质的化学式为________,与C具有相同核外电子排布的粒子有________(至少写出两种).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com