
分析 放热反应指反应物具有的能量高于生成物具有的能量;吸热反应指反应物具有的能量低于生成物具有的能量.
根据常见的放热反应有:所有的物质燃烧、所有金属与酸反应、金属与水反应,所有中和反应;绝大多数化合反应和铝热反应;
常见的吸热反应有:绝大数分解反应,个别的化合反应(如C和CO2),少数分解置换以及某些复分解(如铵盐和强碱).
解答 解:放热反应指反应物具有的能量高于生成物具有的能量;吸热反应指反应物具有的能量低于生成物具有的能量.
①Ba(OH)2•8H20与NH4Cl反应为吸热反应;
②氢气在氧气中燃烧是放热反应;
③氢氧化钾与硫酸中和是放热反应;
④碳酸钙高温分解成氧化钙和二氧化碳为吸热反应;
⑤二氧化碳与赤热的碳反应生成一氧化碳为吸热反应;
⑥锌粒与稀H2S04反应制取H2是放热反应;
故答案为:高于;低于;②③⑥;①④⑤.
点评 本题考查化学反应的热量变化,难度不大,学生应注重归纳中学化学中常见的吸热或放热的反应,对于特殊过程中的热量变化的要熟练记忆来解答此类习题.


 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案科目:高中化学 来源: 题型:选择题
| 选项 | 实验及现象 | 结论 |
| A | 将湿润的红色石蕊试纸放在试管口,试纸变蓝 | 反应中有NH3产生 |
| B | 收集产生的气体并点燃,火焰呈淡蓝色 | 反应中有H2产生 |
| C | 收集气体的同时测得溶液的pH为8.0 | 弱碱性溶液中Mg也可被氧化 |
| D | 将光亮的镁条放入pH为8.6的NaHCO3溶液中,有气泡产生 | 弱碱性溶液中OH-氧化了Mg |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 已知X、Y和Z三种元素的原子序数之和等于48.X是有机物主要组成元素.X的一种1:1型气态氢化物分子中既有σ键又有π键.Z是金属元素,Z的核电荷数小于28,且次外层有2个未成对电子.
已知X、Y和Z三种元素的原子序数之和等于48.X是有机物主要组成元素.X的一种1:1型气态氢化物分子中既有σ键又有π键.Z是金属元素,Z的核电荷数小于28,且次外层有2个未成对电子.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba(OH)2=Ba2++2OH- | B. | NaHCO3=Na++H++CO32- | ||
| C. | NaHSO4=Na++H++SO42- | D. | CH3COOH?CH3COO-+H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 化工厂生产盐酸的主要过程是:
化工厂生产盐酸的主要过程是:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1个 | B. | 2个 | C. | 3个 | D. | 4个 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
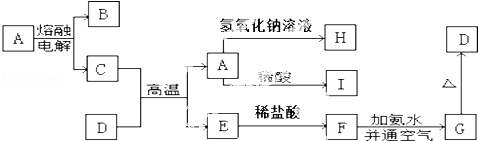
 A、B、C、D、E进行焰色反应均显黄色,这些物质能实现如图所示的转化关系.其中A为淡黄色固体,C为强碱.
A、B、C、D、E进行焰色反应均显黄色,这些物质能实现如图所示的转化关系.其中A为淡黄色固体,C为强碱.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com