
 快捷英语周周练系列答案
快捷英语周周练系列答案科目:高中化学 来源:不详 题型:单选题
| A.A的能量一定高于C的能量 |
| B.B的能量一定高于D的能量 |
| C.反应物A与B的总能量一定低于生成物C与D的总能量 |
| D.反应物A与B的总能量一定高于生成物C与D的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(10分)A―E五种元素中,除A、B外其他均为短周期元素,它们的性质或原子结构如下表:
| 元素 | 元素性质或原子结构 |
| A | 单质为生活中常见的金属,该金属的两种黑色氧化物(其中一种有磁性)的相对分子质量相差160 |
| B | 单质为生活中常见的金属,其相对原子质量比A大8 |
| C | 地壳中含量最多的金属元素 |
| D | 元素的主族序数是其所在周期序数的3倍 |
| E | E的某种原子的原子核内没有中子 |
(1)请写出A在元素周期表中的位置 ;C单质在强碱溶液反应的离子方程式是 。
![]() (2)①在高温条件下,将D、E组成的气态化合物与A的粉末充分反应,生成8gE的单质和 ②A的某种氯化物溶液呈黄色,向其中通入足量SO2气体,溶液变为浅绿色,此反应的离子方程式是 。
(2)①在高温条件下,将D、E组成的气态化合物与A的粉末充分反应,生成8gE的单质和 ②A的某种氯化物溶液呈黄色,向其中通入足量SO2气体,溶液变为浅绿色,此反应的离子方程式是 。
![]() (3)已知化学反应A+2E+=A2++E2能自发进行,若将上述A、
(3)已知化学反应A+2E+=A2++E2能自发进行,若将上述A、
![]() B两种金属,插入含大量E+的电解质溶液的烧杯中,
B两种金属,插入含大量E+的电解质溶液的烧杯中,
![]() 可组成原电池。如图。
可组成原电池。如图。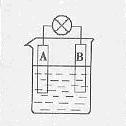
B为_______极,电极反应式为________
查看答案和解析>>
科目:高中化学 来源: 题型:
(10分)A―E五种元素中,除A、B外其他均为短周期元素,它们的性质或原子结构如下表:
元素 | 元素性质或原子结构 |
A | 单质为生活中常见的金属,该金属的两种黑色氧化物(其中一种有磁性)的相对分子质量相差160 |
B | 单质为生活中常见的金属,其相对原子质量比A大8 |
C | 地壳中含量最多的金属元素 |
D | 元素的主族序数是其所在周期序数的3倍 |
E | E的某种原子的原子核内没有中子 |
(1)请写出A在元素周期表中的位置 ;C单质在强碱溶液反应的离子方程式是
(2)①在高温条件下,将D、E组成的气态化合物与A的粉末充分反应,生成8gE的单质和 ②A的某种氯化物溶液呈黄色,向其中通入足量SO2气体,溶液变为浅绿色,此反应的离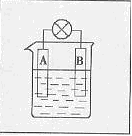 子方程式是 。
子方程式是 。
(3)已知化学反应A+2E+=A2++E2能自发进行,若将上述A、B两种金属,插入含大量E+的电解质溶液的烧杯中,可组成原电池。如图。B为_______极,电极反应式为________
查看答案和解析>>
科目:高中化学 来源:2007-2008学年福建省福州八中高一(下)期末化学试卷(解析版) 题型:选择题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com