
| A. | 红外光谱 | B. | 核磁共振氢谱 | C. | 质谱 | D. | 银镜反应 |
分析 质谱法用于测定有机物的相对分子质量,红外光谱仪用于测定有机物的官能团,紫外光谱鉴别一个有机物是否含有共轭体系或芳香结构,核磁共振氢谱用于测定有机物分子中氢原子的种类和数目;能够发生银镜反应的有机物分子中含有醛基,而质谱法只能确定有机物的相对分子量,据此进行解答.
解答 解:A.红外光谱仪能测定出有机物的官能团和化学键,故A不选;
B.核磁共振氢谱用于测定有机物分子中氢原子的种类和数目,可据此确定有机物结构或官能团,故B不选;
C.质谱法用于测定有机物的相对分子质量,不能测定出有机物的化学键和官能团,故C选;
D.能够发生银镜反应的有机物分子中含有醛基,据此可确定有机物含有官能团或结构,故D不选;
故选C.
点评 本题考查了确定有机物结构的方法,题目难度不大,注意掌握红外光谱、核磁共振氢谱、质谱法含义及应用,试题侧重基础知识的考查,明确确定有机物结构的常用方法为解答关键.


 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:选择题
| 混合物 | 试剂 | 分离方法 | |
| A | 苯(苯酚) | 过量浓溴水 | 过滤 |
| B | 乙烷(乙烯) | 酸性高锰酸钾溶液 | 洗气 |
| C | 溴苯(溴) | 氢氧化钠溶液 | 分液 |
| D | 乙酸乙酯(乙酸) | 饱和碳酸钠溶液 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
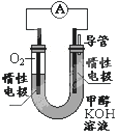 甲醇(CH3OH)是一种可再生能源,具有广泛的开发和应用前景.
甲醇(CH3OH)是一种可再生能源,具有广泛的开发和应用前景.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在NaCl晶体中,与一个Na+最近的且距离相等的Cl-的个数 | |
| B. | 在二氧化硅晶体中,围成最小环的原子数 | |
| C. | 在金刚石晶体中,围成最小环的原子数 | |
| D. | 在CsCl晶体中,与一个Cs+最近的且距离相等的Cs+的个数 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
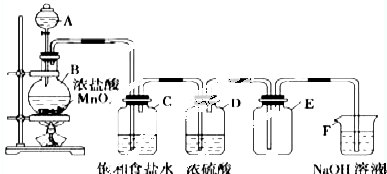
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第ⅠA族元素的金属性比第ⅡA族元素的金属性强 | |
| B. | 第ⅥA族元素中,气态氢化物稳定性最好的其单质氧化性也最强 | |
| C. | 同周期非金属氧化物对应水化物的酸性从左到右依次增强 | |
| D. | 第二周期元素的最高化合价为+1→+7 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
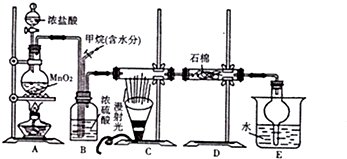
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
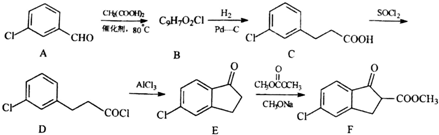
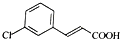 ,由D→E的反应类型是取代反应.
,由D→E的反应类型是取代反应.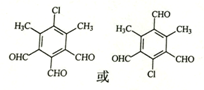 .
.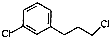 )为原料制备化合物E(
)为原料制备化合物E(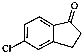 )的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
)的合成路线流程图(无机试剂任用).合成路线流程图示例如下:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com