


分析 (1)依据装置图中的仪器和所盛放试剂判断仪器的名称和作用判断;
(2)氯化铝、乙酸酐都是易水解的物质;
(3)乙酸酐和苯反应剧烈,温度过高会生成更多的副产物;
(4)依据萃取的原理是利用物质在互不相溶的溶剂中 的溶解度不同,对混合溶液进行分离;
(5)蒸馏装置的目的是控制物质的沸点,在一定温度下镏出物质;温度计水银球是测定蒸馏烧瓶支管口处的蒸气温度.
解答 解:(1)仪器a为干燥管,装置b的作用是吸收反应过程中所产生的HCl气体,
故答案为:干燥管;吸收HCl气体;
(2)由于三氯化铝与乙酸酐极易水解,所以要求合成过程中应该无水操作;目的是防止AlCl3和乙酸酐水解,
故答案为:防止三氯化铝和乙酸酐水解;
(3)若将乙酸酐和苯的混合液一次性倒入三瓶颈,可能会导致反应太剧烈,反应液升温过快导致更多的副产物,
故答案为:AD;
(4)水层用苯萃取并分液的目的是把溶解在水中的苯乙酮提取出来以减少损失,由于乙醇能与水混溶不分层,所以不能用酒精代替苯进行萃取操作,
故答案为:把溶解在水中的苯乙酮提取出来以减少损失;否;乙醇易溶于水;
(5)粗产品蒸馏提纯时,温度计的水银球要放在蒸馏烧瓶支管口处,漏斗装置中的温度计位置正确的是C项,若温度计水银球放在支管口以下位置,会导致收集的产品中 混有低沸点杂质;若温度计水银球放在支管口以上位置,会导致收集的产品中混有高沸点杂质;所以A、B项的装置容易导致低沸点杂质混入收集到的产品中,
故答案为:C.
点评 本题考查了物质制备,为高频考点,侧重于学生的分析、实验能力的考查,题目涉及分离、提纯、萃取剂选择、仪器使用等试验基础知识的应用,化学实验基本知识和基本技能的掌握是解题关键,难度中等.


科目:高中化学 来源: 题型:选择题

| A. | 原溶液中c(Fe3+)=0.2mol•L-1 | |
| B. | SO42-、NH4+、Na+一定存在,CO32-一定不存在 | |
| C. | 要确定原溶液中是否含有Fe2+,其操作为取少量原溶液于试管中,加KSCN溶液,再加入适量氯水,溶液呈血红色,则含有Fe2+ | |
| D. | 溶液中至少有4种离子存在,其中Cl-一定存在,且c(Cl-)≥0.2mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 11.1% | B. | 22.2% | C. | 33.3% | D. | 37.8% |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该温度下此反应的平衡常数K=400 | |
| B. | 其他条件不变,再充入0.3mol SO2和0.2mol O2平衡时,SO2的体积分数增大 | |
| C. | 平衡时,SO2的转化率为95% | |
| D. | 前2min SO2的平均反应速率0.02mol/(L•s) |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
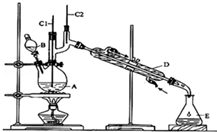 正丁醛是一种化工原料.某实验小组利用如下装置合成正丁醛.
正丁醛是一种化工原料.某实验小组利用如下装置合成正丁醛.| 沸点/℃ | 密度(g•cm-3) | 水中溶解性 | |
| 正丁醇 | 117.2 | 0.8109 | 微溶 |
| 正丁醛 | 75.5 | 0.8107 | 微溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
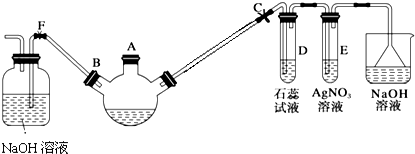
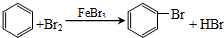 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
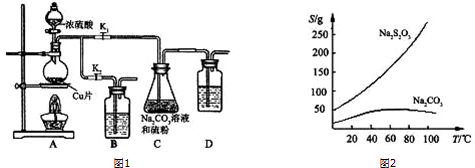
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 12.0% | B. | 14.3% | C. | 19.0% | D. | 66.7% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com