
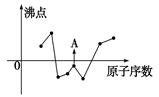
| A.原子最外层电子数:X>Y>Z | B.单质沸点:X>Y>Z |
| C.离子半径:X2->Y+>Z- | D.原子序数:X>Y>Z |
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源:不详 题型:单选题
| A.原子核外电子排布式为1s2的X原子与原子核外电子排布式为1s22s2的Y原子 |
| B.原子核外M层上仅有两个电子的X原子与原子核外N层上仅两个电子的Y原子 |
| C.2p轨道上只有一个空轨道的X原子与3p轨道上只有一个空轨道的Y原子 |
| D.最外层都只有一个电子的X、Y原子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.锂与水反应不如钠与水反应剧烈 |
| B.还原性:K>Na>Li,故 |
| C.容沸点:Li>Na>K |
| D.原子半径:Li<Na<K |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.原子半径大小顺序:r(W)>r(Z)>r(Y)>r(X) |
| B.Y分别与Z、W形成的化合物中化学键类型相同 |
| C.X的最高价氧化物对应水化物的酸性比W的弱 |
| D.Y的气态简单氢化物的热稳定性比W的强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
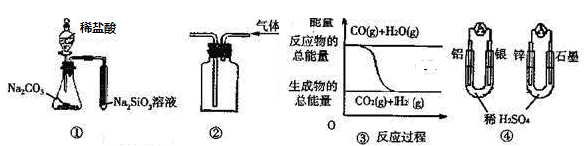
| A.用图 ① 所示实验可比较氯、碳、硅三种元素的非金属性强弱 | |
B.用图 ② 所示实验装置排空气法收集CO2气体 | C.图 ③ 表示反应 CO(g)+H2O(g) CO2(g)+H2(g)是放热反应 |
| D.图 ④ 两个装置中通过导线的电子数相同时,消耗负极材料的物质的量也相同 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 键长/(pm) | B—F | B—Cl | B—Br |
| 计算值 | 152 | 187 | 199 |
| 实测值 | 130 | 175 | 187 |

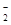 。判断HF
。判断HF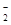 和HF
和HF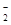 微粒间能否形成氢键,并说明理由。
微粒间能否形成氢键,并说明理由。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com