
| A、锌放入稀硫酸中 |
| B、高锰酸钾分解 |
| C、实验室制备氨气 |
| D、碳和水蒸气在高温下反应 |


科目:高中化学 来源: 题型:
| A、若满足:c(Cl-)=c(NH4+)>c(OH-)=c(H+),则溶质一定是NH4Cl |
| B、若满足:c(NH4+)>c(Cl-)>c(OH-)>c(H+),则溶质一定是NH4Cl和NH3-?H2O |
| C、溶液中四种离子之间可能满足:c(Cl-)>c(H+)>c(NH4+)>c(OH-) |
| D、若满足:c(NH4+)=c(Cl-),则溶液一定呈中性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、x>y | B、x<y |
| C、x=y | D、无法判断 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、铜片增重6.4g |
| B、锌片增重6.5 g |
| C、铜片上析出0.1 mol O2 |
| D、锌片溶解了6.5 g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 放电 |
| 充电 |
| A、电池充电时,Ni(OH)2只作为阴极上反应的原料 |
| B、该反应属于可逆反应 |
| C、电池充电时,氢元素被还原 |
| D、电池放电时,H2是负极 |
查看答案和解析>>
科目:高中化学 来源: 题型:
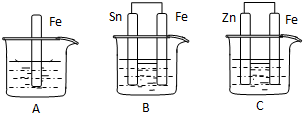 如图所示,烧杯中都盛有稀硫酸.
如图所示,烧杯中都盛有稀硫酸.查看答案和解析>>
科目:高中化学 来源: 题型:
 某学生利用下面实验装置探究盐桥式原电池的工作原理.
某学生利用下面实验装置探究盐桥式原电池的工作原理.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com