
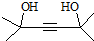 ��
��
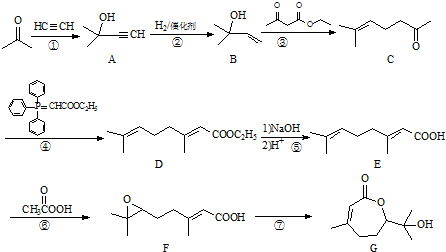
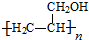 ��д���ϳ�����ͼ�����Լ����ã����ϳ�����ͼʾ�����£�CH2=CH2$\stackrel{HBr}{��}$CH3CH2Br$��_{��}^{NaOH��Һ}$CH3CH2OH��
��д���ϳ�����ͼ�����Լ����ã����ϳ�����ͼʾ�����£�CH2=CH2$\stackrel{HBr}{��}$CH3CH2Br$��_{��}^{NaOH��Һ}$CH3CH2OH�� ���� ��1����G�Ľṹ��ʽ�ж������������ţ�
��2����A��B�Ľṹ��ʽ��֪����Ӧ����̼̼�����������ӳɷ�Ӧ����̼̼˫����
��3����Ӧ���DZ�ͪ����Ȳ���ʻ��ϵļӳɷ�Ӧ�����õ���һ����������ʽΪC8H14O2�����䷢������2mol��ͪ����Ȳ�ļӳɷ�Ӧ��
��4����I�ķ���ʽ��F�Ľṹ��ʽ����I�Ľṹ��ʽ��
��5����G�Ľṹ��ʽ�����������ж�J�Ľṹ��ʽ��
��6����CH3OH��CH��CHΪԭ�Ϻϳɾ۱�ϩ�� 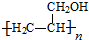 ����Ϸ�Ӧ�ٿ�֪���轫�״�����Ϊ��ȩ��������Ȳ��Ӧ����CH��CCH2OH���������ӳɲ���Ӿۿɵ�
����Ϸ�Ӧ�ٿ�֪���轫�״�����Ϊ��ȩ��������Ȳ��Ӧ����CH��CCH2OH���������ӳɲ���Ӿۿɵ�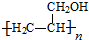 ��
��
��� �⣺��1����G�Ľṹ��ʽ��֪��G�к����������ǻ����ֹ����ţ��ʴ�Ϊ���������ǻ���
��2����Ӧ����̼̼�����������ӳɷ�Ӧ����̼̼˫�����ʴ�Ϊ���ӳɷ�Ӧ��
��3���õ���һ����������ʽΪC8H14O2�����䷢������2mol��ͪ����Ȳ�ļӳɷ�Ӧ��H�Ľṹ��ʽΪ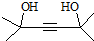 ���ʴ�Ϊ��
���ʴ�Ϊ��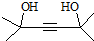 ��
��
��4����Ϊ��״�ṹ������ʽΪC10H18O4����G����I�Ľṹ��ʽΪ ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
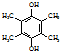
��5��������FeCl3��Һ������ɫ��Ӧ��˵�����б����ͷ��ǻ����ڷ��ӵĺ˴Ź���������2���壬˵��2�����ǻ��ڱ����Ķ�λ�������ϻ���4������J�Ľṹ��ʽΪ ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��6����CH3OH��CH��CHΪԭ�Ϻϳɾ۱�ϩ�� 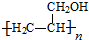 ����Ϸ�Ӧ�ٿ�֪���轫�״�����Ϊ��ȩ��������Ȳ��Ӧ����CH��CCH2OH���������ӳɲ���Ӿۿɵ�
����Ϸ�Ӧ�ٿ�֪���轫�״�����Ϊ��ȩ��������Ȳ��Ӧ����CH��CCH2OH���������ӳɲ���Ӿۿɵ�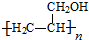 ����ϳ�·��Ϊ
����ϳ�·��Ϊ ��
��
�ʴ�Ϊ�� ��
��
���� ���⿼���л���ĺϳɣ���Ŀ�Ѷ��еȣ������Ҫע����������Ϣ��Ϊ������Ĺؼ������ݷ�Ӧ���������ŵı仯�жϣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 100mL 3.0mol/L��������5.6g��м��ȫ��Ӧת�Ƶĵ�����Ϊ0.3NA | |
| B�� | ��2mol H2SO4��Ũ��������������ͭ��ȫ��Ӧ������SO2����ĿΪNA | |
| C�� | 1L 0.1mol/L Na2CO3��Һ�У�������������Ϊ0.3NA | |
| D�� | 16.0g�Ĺ��������������к��еĵ�����Ϊ9NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
 ��2L�ĺ����ܱ������У�������Ӧ��A��g��+B��g��?2C��g��+D��s����H=-a kJ•mol-1��ʵ�����ݺͽ���ֱ��������ͼ��ʾ������˵����ȷ���ǣ�������
��2L�ĺ����ܱ������У�������Ӧ��A��g��+B��g��?2C��g��+D��s����H=-a kJ•mol-1��ʵ�����ݺͽ���ֱ��������ͼ��ʾ������˵����ȷ���ǣ�������| ʵ�� ��� | �¶� | ��ʼ���ʵ��� | ���� �仯 | |
| A | B | |||
| �� | 600�� | 1 mol | 3 mol | 96 kJ |
| �� | 800�� | 0.5 mol | 1.5mol | -- |
| A�� | ʵ����У�10 min��ƽ������v��B��=0.06 mol•L-1•min-1 | |
| B�� | 600��ʱ����������ʽ��a=160 | |
| C�� | 600��ʱ���÷�Ӧ��ƽ�ⳣ����0.45 | |
| D�� | ��ʵ����ƽ����ϵ���ٳ���0.5 mol A��1.5 mol B��A��ת���ʲ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ɫ��Һ��Cu2+��K+��MnO4-��SO42- | |
| B�� | ���ܽ�Al2O3����Һ��Na+��Ca2+��HCO3-��NO3- | |
| C�� | ������c��OH-��=1��10-13mol•L-1����Һ��NH4+��Al3+��SO42-��Cl- | |
| D�� | ��1.2 mol•L-1 NO3-����Һ��H+��Fe2+��Mg2+��Br- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
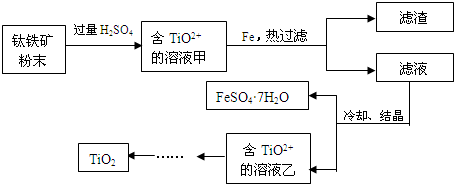
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| ���� | VOSO4 | V2O5 | NH4VO3 | ��VO2��2SO4 |
| �ܽ��� | ���� | ���� | ���� | ���� |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ʯ | B�� | NaOH | C�� | �������� | D�� | ���Ӿ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ˮ | B�� | ����ˮ | C�� | �� | D�� | CCl4 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com