
某离子晶体中晶体结构最小的重复单元如图:A为阴离子,在正方体内,B为阳离子,分别在顶点和面心,则该晶体化学式可能为
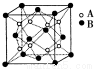
A.CaF2 B.CaO2 C.CaC2 D.Na2O2
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案科目:高中化学 来源:2014-2015学年北京市丰台区高三第二次模拟理综化学试卷(解析版) 题型:选择题
下列说法正确的是
A.用核磁共振氢谱图可以鉴别乙醇和溴乙烷
B.乙烯、苯、乙醇均能使酸性高锰酸钾溶液褪色
C.乙醇可以转化成乙醛,乙醇和乙醛都能发生加成反应
D. 的结构中只含有羟基和羧基
的结构中只含有羟基和羧基
查看答案和解析>>
科目:高中化学 来源:2014-2015浙江省高二4月月考化学试卷(解析版) 题型:选择题
下列关于乙二醇和丙三醇的说法中,不正确的是
A.乙二醇的水溶液凝固点很低,可作汽车发动机的抗冻剂
B.丙三醇的沸点比乙二醇的沸点高,可用于配制化妆品
C.这两种多元醇都易溶于水,但难溶于有机溶剂
D.丙三醇可以制造炸药,乙二醇是制涤纶的主要原料
查看答案和解析>>
科目:高中化学 来源:2014-2015浙江省高二4月月考化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数,下列有关说法正确的是
A.0.5 mol苯分子中含有C=C双键数为1.5 NA
B.1 mol甲基(—CH3)所含的电子总数为10 NA
C.标准状况下,1L甲醇完全燃烧后生成的CO2分子数目约为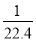 NA
NA
D.2.8 g乙烯和丙烯的混合气体中所含碳原子数为0.2NA
查看答案和解析>>
科目:高中化学 来源:2014-2015山西省太原市高二4月阶段形成检测化学试卷(解析版) 题型:填空题
(11分)
(1)通常人们把拆开1 mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热(△H),化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。
化学键 | Si—O | Si—Cl | H—H | H—Cl | Si—Si | Si—C |
键能/kJ·mol—1 | 460 | 360 | 436 | 431 | 176 | 347 |
请回答下列问题:
①比较下列两组物质的熔点高低(填“>”或“<”=)
SiC Si; SiCl4 SiO2
②下图立方体中心的“●”表示硅晶体中的一个原子,请在立方体的顶点用“●”表示出与之紧邻的硅原子。
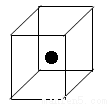
③工业上高纯硅可通过下列反应制取:
SiCl4(g) + 2H2(g) 高温 Si(s) + 4 HCl(g) 该反应的反应热△H = kJ/mol.
(2)化合物Na2O的晶胞如图。
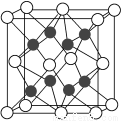
①其中O2-离子的配位数为________,
②该化合物与MgO相比,熔点较高的是________(填化学式)。
③已知该化合物的晶胞边长为a pm,则该化合物的密度为________g·cm-3(只要求列出算式,不必计算出数值,阿伏加德罗常数的数值为NA)。
查看答案和解析>>
科目:高中化学 来源:2014-2015山西省太原市高二4月阶段形成检测化学试卷(解析版) 题型:选择题
下列说法正确的是
A.第二周期元素的第一电离能随原子序数递增依次增大
B.卤族元素中氟的电负性最大
C.CO2、SO2都是直线形的非极性分子
D.CH2=CH2分子中共有四个σ键和一个π键
查看答案和解析>>
科目:高中化学 来源:2014-2015山西省太原市高二4月阶段形成检测化学试卷(解析版) 题型:选择题
在常温常压下呈气态的化合物,降温使其固化得到的晶体属于
A.分子晶体 B.原子晶体
C.离子晶体 D.何种晶体无法判断
查看答案和解析>>
科目:高中化学 来源:2014-2015浙江省高二下学期4月阶段性测试化学试卷(解析版) 题型:选择题
一定温度下,pH=a的某电解质溶液中,插入两支惰性电极通直流电一段时间后,溶液的pH<a,则该电解质可能是
A.NaCl B.H2SO4 C.CuCl2 D.Na2SO4
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东齐鲁名校教科研协作体19所名校高三第二次调研化学试卷(解析版) 题型:填空题
(12分)A、B、C、D、E、F六种短周期主族元素,其原子序数依次增大,其中B与C同周期,D与E和F同周期,A与D同主族,C与F同主族,C元素的原子最外层电子数是次外层电子数的三倍,D是所在周期原子半径最大的主族元素。又知六种元素所形成的常见单质在常温常压下有三种是气体,三种是固体。
请回答下列问题:
(1)元素F在周期表中的位置________。
(2)C、D、F三种元素形成的简单离子的半 径由大到小的顺序是(用离子符号表示)________。
径由大到小的顺序是(用离子符号表示)________。
(3)由A、B、C三种元素以原子个数比4:2:3形成化合物X,X中所含化 学键类型有______。检验该化合物中的阳离子的方法是________(用离子方程式表示)。
学键类型有______。检验该化合物中的阳离子的方法是________(用离子方程式表示)。
(4)若E是金属元素,其单质与氧化铁反应常用于焊接钢轨,请写出D元素的最高价氧化物对应的水化物与E的最高价氧化物反应的离子方程式:________________________。若E是非金属元素,其单质在电子工业中有重要应用,请写出其单质溶于强碱溶液的离子方程式:_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com