
分析 (1)依据热化学方程式和盖斯定律计算得到;
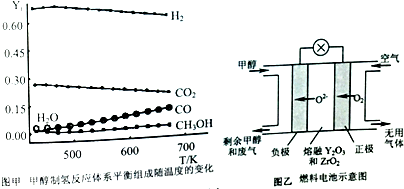
(2)①A、依据图象分析甲醇体积分数很小,说明转化率高;
B、生成氢气的反应Ⅱ、Ⅲ都是放热反应,升温反应逆向进行,氢气量减小;
C、低温有利于氢气生成,但反应速率小,寻找催化剂可以提高反应速率;
②反应ⅡCO(g)+H2O(g)=CO2(g)+H2(g)△H=-43.5kJ•mol-1 ,依据平衡三段式列式计算转化率,依据浓度商和平衡常数比较判断反应进行的方向;
(3)燃料电池中燃料在负极失电子发生氧化反应,电解质是熔融金属氧化物,甲醇失电子生成二氧化碳.
解答 解:(1)①SO2(g)+I2(g)+2H2O(g)=2HI (g)+H2SO4(l)△H=a kJ•mol-1
②2H2SO4(l)=2H2O(g)+2SO2(g)+O2(g)△H=b kJ•mol-1
③2HI(g)=H2(g)+I2(g)△H=c kJ•mol-1
依据盖斯定律①×2+②+③×2得到2H2O(g)=2H2(g)+O2(g)△H=(2a+b+2c)KJ/mol,故答案为:(2a+b+2c);
(2)①A、依据图象分析,在0.1MPa、473~673K温度范围内甲醇体积分数很小,说明转化率高,故A正确;
B、生成氢气的反应Ⅱ、Ⅲ都是放热反应,升温反应逆向进行,氢气量减小,故B错误;
C、低温有利于氢气生成,但反应速率小,寻找催化剂可以提高反应速率,寻找在较低温度下的催化剂在本制氢工艺中至关重要,故C正确:
故答案为:AC;
②依据化学平衡三段式计算列式得到,设CO反应量为x,气体体积为v
CO(g)+H2O(g)=CO2(g)+H2(g)
起始量(mol) 1 3 0 0
变化量(mol) x x x x
平衡量(mol) 1-x 3-x x x
K=$\frac{\frac{n(C{O}_{2})}{V}×\frac{n({H}_{2})}{V}}{\frac{n(CO)}{V}×\frac{n({H}_{2}O)}{V}}$=$\frac{{x}^{2}}{(1-x)(3-x)}$=1
x=0.75
CO转化率=75%;
平衡常数随温度变化,不随浓度改变,反应达到平衡后再向其中加入1.0mol CO、1.0mol H2O、1.0mol CO2和1.0mol H2,则
CO(g)+H2O(g)=CO2(g)+H2(g)
1-0.75+1 3-0.75+1 0.75+1 0.75+1
Qc=$\frac{1.7{5}^{2}}{1.25×3.25}$=0.75<K,反应正向进行,正反应速率>逆反应速率,
故答案为:75%;>;
(3)甲醇作燃料的电池示意图中电解质是金属氧化物,甲醇失电子结合氧离子生成二氧化碳,结合电子守恒原子守恒写出负极电极反应为:CH3OH-6e-+3O2-=CO2↑+2H2O,
故答案为:CH3OH-6e-+3O2-=CO2↑+2H2O.
点评 本题考查了热化学方程式和盖斯定律的计算应用,化学平衡影响因素的分析判断,三段式计算的应用,平衡常数计算与计算分析,原电池电极反应书写方法,题目难度中等.


科目:高中化学 来源: 题型:解答题
| 投料比 CO的体积分数% 温度/℃ | $\frac{n({H}_{2}O)}{n(CO)}$=1 | $\frac{n({H}_{2}O)}{n(CO)}$=3 | $\frac{n({H}_{2}O)}{n(CO)}$=5 |
| 200 250 300 350 | 1.70 2.73 6.00 7.85 | 0.21 0.30 0.84 1.52 | 0.02 0.06 0.43 0.80 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.125 | B. | 0.10 | C. | 0.08 | D. | 0.20 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钠溶液盛装在玻璃塞的试剂瓶中 | |
| B. | 新制氯水保存在无色广口瓶中 | |
| C. | 铝片密封保存在细口瓶中 | |
| D. | 金属钠保存在煤油中 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 离子晶体 | 原子晶体 | 分子晶体 | |
| A | NaOH | Ar | SO2 |
| B | H2SO4 | 石墨 | S |
| C | CH3COONa | 水晶 | 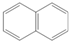 |
| D | Ba(OH)2 | 金刚石 | 玻璃 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- | |
| B. | 加入氢氧化钠溶液,先产生白色沉淀,后迅速变为灰绿色,最后变为红褐色,一定有Fe2+ | |
| C. | 加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32- | |
| D. | 加入硝酸银溶液产生白色沉淀,再加稀硝酸,白色沉淀不溶解,一定有Ag+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com