
| A. | 2.3g钠与水反应失去的电子数目为0.2NA | |
| B. | 20℃、101KPa时,5.6L NH3 所含的原子数目为NA | |
| C. | 10℃、101KPa时,16g CH4 所含有的电子数为10NA | |
| D. | 1mol NaCl固体溶于1L水所得的溶液中NaCl的物质的量浓度为1 mol•L-1 |
分析 A、求出钠的物质的量,然后根据1mol钠反应失去1mol电子来分析;
B、20℃、101KPa时,气体摩尔体积大于22.4L/mol;
C、求出甲烷的物质的量,然后根据1mol甲烷中含10mol电子来分析;
D、将氯化钠溶于1L水中,溶液体积大于1L.
解答 解:A、2.3g钠的物质的量为0.1mol,而1mol钠反应失去1mol电子,故0.1mol钠失去0.1NA个电子,故A错误;
B、20℃、101KPa时,气体摩尔体积大于22.4L/mol,故5.6L氨气的物质的量小于0.25mol,则含有的原子小于NA个,故B错误;
C、16g甲烷的物质的量为1mol,而1mol甲烷中含10mol电子,故含10NA个,故C正确;
D、将氯化钠溶于1L水中,溶液体积大于1L,故所得溶液中氯化钠的浓度小于1mol/L,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.


科目:高中化学 来源: 题型:选择题
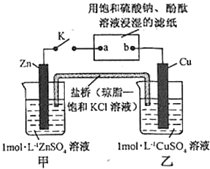
| A. | Cu 电极上发生还原反应 | B. | 电子沿 Zn→a→b→Cu 路径流动 | ||
| C. | 片刻后甲池中 c(SO42-)增大 | D. | 片刻后可观察到滤纸 b 点变红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (CH3)3COH的名称:2,2二甲基乙醇 | B. | 乙醛的结构式:CH3CHO | ||
| C. | CH4分子的比例模型: | D. | 丙烯分子的结构简式为 CH3CHCH2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放电时,蓄电池内电路中H+向负极移动 | |
| B. | 放电时,每通过lmol电子,蓄电池就要消耗2molH2SO4 | |
| C. | 充电时,阳极反应:PbSO4+2e-→Pb+SO42- | |
| D. | 充电时,铅蓄电池的负极与外接电源的负极相连 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铍原子的半径小于硼原子的半径 | |
| B. | 相同条件下,单质铍与酸反应比单质锂与酸反应剧烈 | |
| C. | 氢氧化铍的碱性比氢氧化钙的碱性弱 | |
| D. | 单质铍能与冷水剧烈反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用氯化铝和纯硝酸反应 | |
| B. | 氯化铝与氢氧化钠反应,过滤得沉淀,再加稀HNO3 | |
| C. | 用AlCl3溶液和氨水反应,过滤得沉淀,再加稀HNO3 | |
| D. | AlCl3溶液和Ba(NO3)2溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
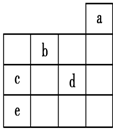
| A. | 元素b位于VIA族,有+6、-2两种常见化合价 | |
| B. | 元素的最高价氧化物对应的水化物的酸性:d>c>e | |
| C. | 金属性c>e | |
| D. | 元素的气态氢化物的稳定性:e>c>d |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 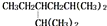 的系统命名法为2,5-二甲基-4-乙基己烷 的系统命名法为2,5-二甲基-4-乙基己烷 | |
| B. | 羟基(-OH)和氢氧根(OH-)所含电子数相等 | |
| C. | 总质量一定时,乙酸和葡萄糖无论以何种比例混合,完全燃烧消耗氧气的量相等 | |
| D. | 油脂、淀粉、蛋白质等高分子化合物都属于混合物,一定条件下均可发生水解 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 当5NA个电子转移时,该反应放出650 kJ的热量 | |
| B. | 当1NA个水分子生成且为气体时,放出多于1300 kJ的热量 | |
| C. | 当2 NA个碳氧双键生成时,放出1300 kJ的热量 | |
| D. | 当4NA个碳氧共用电子对生成时,放出1300kJ的热量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com