
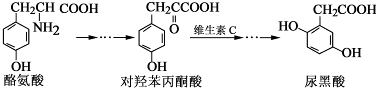
| A. | 对羟基苯丙酮酸分子中在同一平面上的碳原子至少有7个 | |
| B. | 1 mol尿黑酸与足量浓溴水反应,最多消耗3molBr2 | |
| C. | 酪氨酸既能与盐酸反应,又能与氢氧化钠反应 | |
| D. | 1 mol尿黑酸与足量NaHCO3反应,最多消耗3 molNaHCO3 |
分析 A.对羟基苯丙酮酸中苯环为平面结构,与苯环直接相连的C原子一定在同一平面内;
B.尿黑酸中含酚-OH,酚-OH的邻、对位与溴水发生取代反应;
C.酪氨酸中含酚-OH和氨基,具有酸性和碱性;
D.尿黑酸中只有-COOH与NaHCO3反应.
解答 解:A.对羟基苯丙酮酸中苯环为平面结构,与苯环直接相连的C原子一定在同一平面内,所以同一平面上的碳原子至少有7个,故A正确;
B.尿黑酸中含酚-OH,酚-OH的邻、对位与溴水发生取代反应,则1 mol尿黑酸与足量浓溴水反应,最多消耗3 mol Br2,故B正确;
C.酪氨酸中含酚-OH和氨基,具有酸性和碱性,则既能与盐酸反应,又能与氢氧化钠反应,故C正确;
D.尿黑酸中只有-COOH与NaHCO3反应,则1 mol尿黑酸与足量NaHCO3反应,最多消耗1mol NaHCO3,故D错误;
故选D.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重酚、羧酸性质的考查,注意选项C共面问题为解答的易错点,题目难度中等.


科目:高中化学 来源: 题型:选择题

| A. | 供电时的总反应为2H2+O2=2H2O | |
| B. | 负极电极反应为2H2+4OH--4e-=4H2O | |
| C. | 正极电极反应为O2+2H2O+4e-=4OH- | |
| D. | 该燃料电池的能量转化率可达100% |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al2O3→Al(OH)3 | B. | CaCO3→Ca(OH)2 | C. | CH3CH2OH→CH3CHO | D. | CO→Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | n(Fe)<n(S),总质量等于44 g | B. | n(Fe)>n(S),总质量小于44 g | ||
| C. | n(Fe)=n(S),总质量大于44 g | D. | n(Fe)>n(S),总质量等于44 g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸铝溶液中加入过量的氨水:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | |
| B. | 金属钠投入水中:Na+H2O═Na++OH-+H2↑ | |
| C. | 将铝片放入过量NaOH溶液中:2Al+2OH-+2H2O═2AlO2-+3H2↑ | |
| D. | 氧化铝溶于NaOH溶液:Al2O3+2OH-═2AlO2-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 基态原子含有未成对电子最多的第二周期元素 | |
| B. | 位于周期表中第三周期第ⅢA族的元素 | |
| C. | 基态原子最外电子层排布为2s22p6的元素 | |
| D. | 基态原子最外电子层排布为3s23p5的元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com