
| A、在一定浓度的氯水中加小苏打有气泡生成 |
| B、新制氯水中只存在2个平衡状态 |
| C、氯水应保存在棕色瓶中,久置的氯水,PH值减小 |
| D、饱和氯水与石灰石的反应是制取较浓HClO溶液的重要方法 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、配制银氨溶液时是将硝酸银溶液滴入到氨水中至不再生成沉淀为止 |
| B、容量瓶和中和滴定用的锥形瓶用蒸馏水洗净后立即使用,不会对实验结果造成误差 |
| C、检验二氧化硫气体中是否含有二氧化碳,可以将气体通入到饱和碳酸氢钠溶液中 |
| D、为准确测定盐酸与NaOH溶液反应的中和热,所用酸和碱的物质的量应相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
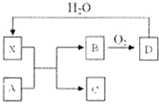 已知X为一种常见酸的浓溶液,能使蔗糖粉末变黑.A与X反应的转化关系如图所示,其中反应条件及部分产物均已略去,则下列有关说法正确的是( )
已知X为一种常见酸的浓溶液,能使蔗糖粉末变黑.A与X反应的转化关系如图所示,其中反应条件及部分产物均已略去,则下列有关说法正确的是( )| A、X使蔗糖变黑的现象主要体现了X的强氧化性 |
| B、若A为铁,则足量A与X在室温下即可完全反应 |
| C、若A为碳单质,则将C通入少量的澄清石灰水,一定可以观察到白色沉淀产生 |
| D、工业上,B转化为D的反应条件为450℃、常压、使用催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、2SO2+O2
| ||||
| B、N2(g)+2O2(g)=2NO2(g)△H=+67.7kJ/mol | ||||
| C、C(s)+O2(g)=CO2(g)△H=+393.5kJ/mol | ||||
D、H2O(l)═H2(g)↑+
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2.0×10-7 mol?L-1 |
| B、0.1×10-7 mol?L-1 |
| C、5×10-8mol?L-1 |
| D、无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、亚硝酸盐有强氧化性 |
| B、普通血红蛋白有较强氧化性 |
| C、亚硝酸盐中毒后,使用美蓝,高铁血红蛋白被还原 |
| D、中毒与解毒过程中都发生了氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com