
下列关于化学基本概念和基本理论的几点认识中正确的是
A.胶体区别于其它分散系的本质特征是具有丁达尔现象
B.碱性氧化物一定是金属氧化物,金属氧化物不一定是碱性氧化物
C.根据化合物中含氢数目的多少,把化合物分为一元酸、二元酸、三元酸等
D.任何无机化学反应一定属于四大基本反应类型之一
科目:高中化学 来源: 题型:
已知3.2g某气体中含有3.01×1022个分子,此气体的摩尔质量是( )
|
| A. | 32 g/mol | B. | 64 | C. | 64 g/mol | D. | 4 g |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知CO和H2的混合气体称为水煤气,可由碳与水蒸气在高温下反应生成。如下图:
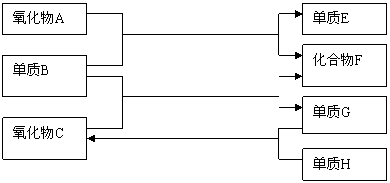
高温
反应①

 高温
高温
反应②
燃烧
反应③
已知:单质E可作为半导体材料,化合物F是有毒的氧化物,C为液态。据此,请填空:
(1)氧化物A是
(2)化合物F是
(3)反应②的化学方程式是
(4)反应③的化学方程式是
查看答案和解析>>
科目:高中化学 来源: 题型:
组成中含有氢氧根的盐叫做碱式盐,酸根中含有氢元素的盐叫酸式盐。下列盐中,既不是碱式盐,也不是酸式盐的是( )
A、NaHSO4 B、Cu2(OH)2CO3 C、Ca(H2PO4)2 D、NH4NO3
查看答案和解析>>
科目:高中化学 来源: 题型:
分类方法在化学学科的发展中起到重要的作用,下列分类标准合理的是
A.根据纯净物的元素组成,将纯净物分为单质和化合物
B.根据物质的元素组成,将物质分为纯净物和混合物
C.根据是否具有丁达尔效应,将分散系分为溶液、浊液和胶体
D.根据反应中的能量变化,将化学反应分为“化合、分解、复分解、置换”四类
查看答案和解析>>
科目:高中化学 来源: 题型:
有关杂化轨道的说法不正确的是
A.杂化前后的轨道数不变,但轨道的形状发生了改变
B.sp3、sp2、sp杂化轨道的夹角分别为109°28′、120°、180°
C.四面体形、三角锥形、V形分子的结构可以用sp3杂化轨道解释
D.杂化轨道全部参加形成化学键
查看答案和解析>>
科目:高中化学 来源: 题型:
硅是重要的半导体材料,构成了现代电子工业的基础。请回答下列问题:
(1)基态Si原子价电子排布图为 ,Si原子核外共有 个不同运动状态的电子。
(2)单质硅存在与金刚石结构类似的晶体,其中原子与原子之间以 相结合,其晶胞中共有8个原子,其中在面心位置贡献 个原子。
(3)单质硅可通过甲硅烷(SiH4)分解反应来制备。工业上采用Mg2Si和NH4Cl在液氨介质中反应制得SiH4,该反应的化学方程式为 。
(4)在硅酸盐中,SiO4- 4四面体(如下图(a))通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(b)为一种无限长单链结构的多硅酸根,其中Si原子的杂化形式为 ,Si与O的原子数之比为 ,化学式为 。

查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示装置,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近溶液呈红色。请回答:
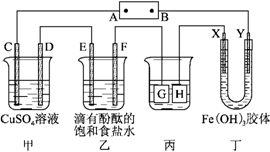 |
(2)若甲、乙装置中的C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为___________________________________。
(3)现用丙装置给铜件镀银,则H应该是_______________(填“镀层金属”或“镀件”),电镀液是______________溶液。当乙中溶液的pH=13时(此时乙溶液体积为500 mL),丙中镀件上析出银的质量为___________________。
(4)丁中X极附近的颜色逐渐变浅,Y极附近的颜色逐渐变深,这表明__________________________,在电场作用下向Y极移动。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com