
【题目】某类化学反应可用如下通式表示:A+B→C+D+H2O 请按要求回答问题:
(1)若C的稀溶液显蓝色,D为红棕色气体,则B溶液的名称是______________,反应中每生成1 mol H2O时转移的电子数目为_________。(以NA表示阿伏加德罗常数的值)
(2)若A为单质,C、D都是能使澄清石灰水变浑浊的气体。则B的化学式为_____________,A、B在化学反应方程式中化学计量数之比为__________________。
(3)若A为氧化物,C、D中有一种是常见的有毒气体单质。该反应的离子方程式为______________________。
(4)若C是一种碱性气体,能使湿润的红色石蕊试纸变蓝,D是一种固体可作干燥剂(中性),则实验室制取气体C的反应的化学方程式是 。
【答案】(1)浓硝酸;6.02×1023(或NA)
(2)H2SO4;1:2
(3)MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
(4)Ca(OH)2+2NH4Cl![]() CaCl2+2NH3↑+2H2O
CaCl2+2NH3↑+2H2O
【解析】
试题分析:(1)若C的稀溶液显蓝色,D为红棕色气体,上述反应为铜和浓硝酸的反应,方程式为Cu+4HNO3═Cu(NO3)2+2NO2↑+2H2O则B溶液的名称是浓硝酸;反应中每生成1 mol H2O时转移的电子数目为6.02×1023(或NA);(2)能使澄清的石灰水变浑浊的气体有和,应为碳和浓硫酸的反应,A呈固态,应为C,则B为浓硫酸,化学式为H2SO4,方程式为C+ 2H2SO4=CO2+2SO2+2H2O;(3)若A为氧化物,C、D中有一种是常见的有毒气体单质,为二氧化锰、浓盐酸反应生成二氧化锰、氯气和水 ,该反应的离子方程式为MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O;(4)碱性气体为NH3,为NH4Cl和Ca(OH)2的反应生成氯化钙、氨气、水,实验室制取氨气的反应的化学方程式是Ca(OH)2 + 2NH4Cl
Mn2++Cl2↑+2H2O;(4)碱性气体为NH3,为NH4Cl和Ca(OH)2的反应生成氯化钙、氨气、水,实验室制取氨气的反应的化学方程式是Ca(OH)2 + 2NH4Cl ![]() CaCl2 + 2NH3↑+ 2H2O。
CaCl2 + 2NH3↑+ 2H2O。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】已知: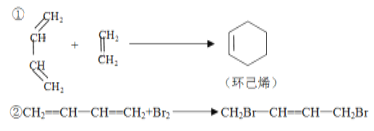
(1)写出下列反应产物的结构简式:
H2C=CHCH=CHCH3+H2C=CHCHO→ _______________。
(2)以某链烃A为起始原料合成化合物G 的路径如下(图中 Mr 表示相对分子质量)
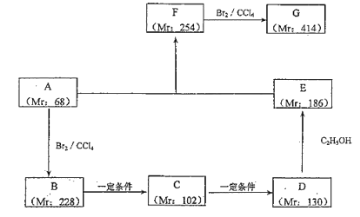
①写出反应类型 B→C:_______,F→G:_______。
②写出下列物质的结构简式:A:________,F:_______。
③写出下列反应的化学方程式:
B→C:________________;D→E:_______________。
④写出 G 与氢氧化钠溶液反应的方程式____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究或认识物质的化学性质一般可从以下几个方面入手(以SiO2为例):
(1)从物质类别角度分析可能具有的通性,如酸性、碱性等。
SiO2属于________氧化物(填“酸性”“碱性”或“两性”)。盛装NaOH等碱性溶液的试剂瓶不能用玻璃塞,其原因可用离子方程式表示为________。
(2)从核心元素化合价角度分析可能具有的氧化性、还原性。
据SiO2中Si元素的价态可推知SiO2________(填字母):
A.只有还原性 B.只有氧化性 C.既有还原性又有氧化性。
工业上用石英砂和焦炭混合高温制取含少量杂质的粗硅,写出该反应的化学方程式________。
(3)从其他角度认识可能具有的特性。
SiO2能与唯一的酸________(填物质名称)反应,工艺上常利用该反应________(填一种用途)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室里需用480mL 0.1mol·L-1的硫酸铜溶液,现选取500mL容量瓶进行配制,以下操作正确的是( )
A. 称取7.68g硫酸铜,加入 500mL水
B. 称取12.0g胆矾配成500mL溶液
C. 称取8.0g硫酸铜,加入500mL水
D. 称取12.5g胆矾配成500mL溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子组在一定条件下能共存,当加入相应试剂后会发生化学变化,且所给离子方程式正确的是( )
选项 | 离子组 | 加入试剂 | 加入试剂后发生反应的离子方程式 |
A | Fe2+、NO | 稀硫酸 | 3Fe 2++NO |
B | Fe3+、I-、ClO- | 氢氧化钠溶液 | Fe3++3OH-= Fe(OH)3↓ |
C | Ba2+、HCO | 氢氧化钠溶液 | HCO |
D | Al3+、Cl-、NO | 过量氢氧化钠溶液 | Al3++3OH-= Al(OH)3↓ |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质均含有某种短周期常见元素,A、G为非金属单质,A常温下为黑色固体,G为空气的主要成份之一;D常温下为无色液体,C、E常温下均为气体,E是形成酸雨的元凶,相对分子质量是G的2倍;F常温下为淡黄色固体。它们的转化关系如图所示。

(1)写出化学式: B________ 、 F________。
(2)写出下列反应的化学方程式:
①:_____________________________________________________________;
②:_____________________________________,并用双线桥法标出反应②中的电子转移情况。
③:___________________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】太阳能的开发利用在新能源研究中占据重要地位,单晶硅太阳能电池片在加工时,一般掺杂微量的铜、锎、硼、镓、硒等。回答下列问題:
⑴二价铜离子的电子排布式为 ,已知高温下Cu2O比CuO更稳定,试从铜原子核外电子结构变化角度解释 。

⑵如图是铜的某种氧化物的晶胞结构示意图,可确定该晶胞中阴离子的个数为 。
⑶往硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+配离子。已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是 。
⑷铜与类卤素(SCN)2反应生成Cu(SCN)2,1mol(SCN)2中含有π键的数目为 ,类卤素(SCN)2对应的酸有两种,理论上硫氰酸(H—S—C≡N)的沸点低于异硫氰酸(H—N=C=S)的沸点。其原因是 。
⑸硼元素具有缺电子性,其化合物可与具有孤电子对的分子或离子形成配合物,如BF3能与NH3反应生成BF3NH3,在BF3NH3中B原子的杂化方式为 ,B与N之间形成配位键,氮原子提供 。
⑹六方氮化硼晶体结构与石墨晶体相似,层间相互作用为 。六方氮化硼在高温高压下,可以转化为立方氮化硼,其结构和硬度都与金刚石相似,晶胞结构如下图所示,晶胞边长为361.5pm,立方氮化硼的密度是 g/cm3。(只要求列算式)。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com