
【题目】酸、碱、盐均属于电解质,它们的水溶液中存在各种平衡.
(1)氨水是中学常见的碱溶液 ①下列事实可证明NH3H2O是弱碱的是(填字母序号).
A.常温下,0.1molL﹣1氨水pH为11
B.氨水能跟氯化亚铁溶液反应生成氢氧化亚铁
C.常温下,0.1molL﹣1氯化铵溶液的pH为5
D. 铵盐受热易分解
②下列方法中,可以使氨水电离程度增大的是(填字母序号).
A.加入少量氯化铁固体 B.通入氨气
C.加入少量氯化铵固体 D.加水稀释
(2)盐酸和醋酸是中学常见酸 用0.1molL﹣1NaOH溶液分别滴定体积均为20.00mL、浓度均为0.1molL﹣1的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入NaOH溶液体积而变化的两条滴定曲线.
①滴定醋酸的曲线是(填“I”或“II”).
②滴定开始前,三种溶液中由水电离出的c(H+)最大的是 .
③V1和V2的关系:V1V2(填“>”、“=”或“<”).
④M点对应的溶液中,各离子的物质的量浓度由大到小的顺序是 .
(3)常温下将0.2mol/L HCl溶液与0.2mol/L氨水溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=6,求混合溶液中下列算式的精确计算结果(填具体数字): c(H+)﹣c(NH3﹒H2O)=mol/L.
(4)铵盐和氯化银是中学常见盐 ①0.1molL﹣1的(NH4)2Fe(SO4)2溶液,与同浓度的(NH4)2SO4溶液相比较(填溶质的化学式)溶液中NH4+的浓度更大,其原因是
②含有足量AgCl固体的饱和溶液,AgCl在溶液中存在如下平衡:
AgCl(s)Ag+(aq)+Cl﹣(aq)
在25℃时,AgCl的Ksp=1.8×10﹣10 . 现将足量AgCl分别放入下列液体中:
①100mL蒸馏水
②100mL 0.3molL﹣1AgNO3溶液
③100mL 0.1molL﹣1 MgCl2溶液
充分搅拌后冷却到相同温度,Ag+浓度由大到小的顺序为(填序号).
【答案】
(1)AC; BC
(2)I;0.1mol?L﹣1醋酸溶液;<; c(CH3COO﹣)>c (Na+)>c (H+)>c (OH﹣)
(3)10﹣8
(4)(NH4)2Fe(SO4)2; NH4+和Fe2+都水解呈酸性,水解相互抑制;②>①>③
【解析】解:(1)①A.常温下,0.1molL﹣1氨水pH为11,溶液呈酸性,说明一水合氨部分电离,则说明一水合氨是弱电解质,故A正确;
B.氨水和氯化亚铁反应生成氢氧化亚铁沉淀,说明一水合氨是碱,但不能说明一水合氨部分电离,所以不能说明是弱电解质,故B错误;
C.常温下,0.1mol/L的氯化铵溶液pH约为5,溶液呈酸性,说明氯化铵是强酸弱碱盐,则说明一水合氨是弱电解质,故C正确;
D.铵盐受热易分解说明铵盐不稳定,不能说明一水合氨部分电离,则不能说明一水合氨是弱电解质,故D错误;
所以答案是:AC;
②A.加入少量氯化铁固体,会消耗氢氧根离子,则促进一水合氨的电离,电离程度增大,故A正确;
B.通入氨气,氨水的浓度增大,电离程度减小,故B错误;
C.加入少量氯化铵固体,铵根离子浓度增大,抑制氨水的电离,电离程度减小,故C错误;
D.加水稀释,促进一水合氨的电离,电离程度增大,故D正确;
所以答案是:AD;(2)①由图中未加NaOH时的pH可知,图Ⅰ中酸的pH大于1,图Ⅱ中酸的pH=1,说明Ⅱ为0.1mol/L的盐酸溶液,为醋酸溶液滴定过程,所以滴定醋酸的曲线是I,
所以答案是:I;
②0.1molL﹣1 NaOH溶液、0.1molL﹣1的盐酸中氢离子和氢氧根浓度都是0.1mol/L,对水的抑制作用一样,但是0.1mol/L醋酸溶液中氢离子浓度小于0.1mol/L,所以对水的电离抑制较小,即三种溶液中由水电离出的c(H+)最大的是0.1 molL﹣1醋酸溶液,所以答案是:0.1molL﹣1醋酸溶液;
③醋酸和氢氧化钠之间的反应,当恰好完全反应得到的醋酸钠显示碱性,要使得溶液显示中性,pH=7,需要醋酸稍过量,所以盐酸和氢氧化钠恰好完全反应,得到的氯化钠显示中性,所以V1<V2,所以答案是:<;
④用0.1molL﹣1 NaOH溶液10mL和溶液体积为20.00mL0.1molL﹣1的醋酸反应,得到的是醋酸和醋酸钠的混合物,显示酸性,此时离子浓度大小c(CH3COO﹣)>c (Na+)>c (H+)>c (OH﹣),所以答案是:c(CH3COO﹣)>c (Na+)>c (H+)>c (OH﹣);(3)根据电荷守恒得c(Cl﹣)+c(OH﹣)=c(NH4+)+c(H+),物料守恒c(NH4+)+c(NH3﹒H2O)=0.1mol/L=c(Cl﹣),
所以c(H+)﹣c(NH3﹒H2O)=c(OH﹣)=10﹣8mol/L,
所以答案是:10﹣8;(4)①:(NH4)2Fe(SO4)2中NH4+和Fe2+都水解呈酸性,水解相互抑制,因此(NH4)2Fe(SO4)2中NH4+的水解程度(NH4)2SO4的要小,(NH4)2Fe(SO4)2比(NH4)2SO4的c(NH4+)大.
所以答案是:(NH4)2Fe(SO4)2;NH4+和Fe2+都水解呈酸性,水解相互抑制;
②氯化银饱和溶液中存在沉淀溶解平衡:AgCl(s)Ag+(ag)+Cl﹣(ag),溶液中c(Ag+)或c(Cl﹣)浓度越大,AgCl溶解度越小,
①100mL蒸馏水中c(Ag+)= ![]() mol/L;
mol/L;
②100mL 0.3molL﹣1AgNO3溶液,c(Ag+)=0.3mol/L;
③100mL0.1molL﹣1MgCl2溶液中,c(Cl﹣)=0.2mol/L,c(Ag+)=9×10﹣10mol/L;
c(Ag+)由大到小的顺序为②>①>③,
所以答案是:②>①>③.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】(1)![]() 的命名为_________________;
的命名为_________________;
(2)分子式为C4H8的烯烃中带有支链的烯烃的结构简式为______________,将该烯烃通入溴的四氯化碳溶液中,发生的反应类型为_______________,该烯烃在一定条件下发生加聚反应的化学方程式为__________________。
(3)乙醇分子中所含官能团的电子式为_______________,请写出与乙醇相对分子质量相等的羧酸和乙醇发生酯化反应的化学方程式__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表中根据实验操作和现象所得出的结论正确的是( )
选项 | 实验操作 | 实验现象 | 实验结论 |
A | 蘸有浓氨水的玻璃棒靠近X | 有白烟产生 | X一定是浓盐酸 |
B | KIO3溶液中加入HI溶液,并加入淀粉 | 溶液变蓝色 | KIO3的氧化性比I2的强 |
C | 强酸性溶液Y中加入Ba(NO3)2溶液,静置后再加入KSCN溶液 | 先有白色沉淀,后溶液又变红 | Y中一定含有SO |
D | C2H5OH与浓硫酸混合后加热到170 ℃ | 制得的气体使酸性KMnO4溶液褪色 | 一定是制得的乙烯使酸性KMnO4溶液褪色 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.下表为元素周期表的一部分,请按要求回答问题:
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ① | ② | ③ | ④ | ⑤ | |||
3 | ⑥ | ⑦ | ⑧ | ⑨ |
(1)表中元素______的非金属性最强,元素_____的金属性最强(填元素符号)。
(2)表中元素④、⑨形成的氢化物的稳定性顺序为_____>______(填化学式)。
(3)表中元素③、④、⑥、⑦的原子半径大小为____>____>___>___(填元素符号)。
Ⅱ.A、B、W、D、E为短周期元素,且原子序数依次增大,五种元素核内质子数之和为39,B、W同周期,A、D同主族,A、W能形成两种液态化合物A2W和A2W2,E元素的周期序数与主族序数相等。
(1)A2W的电子式为________。(2) E元素在周期表中的位置为_______ 。
(3)W、D、E三种元素的简单离子半径由小到大的顺序为_______(填离子符号)。
(4)在一定条件下,D元素的单质能与A元素的单质化合生成DA,DA能与水反应放氢气,则其化学方程式为_______
(5)若要比较D和E的金属性强弱,下列实验方法可行的是_______。
a.将D单质置于E的盐溶液中,若单质D不能置换出单质E,说明D的金属性弱
b.将少量D、E的单质分别投入到水中,若D反应而E不反应,说明D的金属性强
C.比较相同条件下D和E的最高价氧化物对应水化物的溶解性若前者比后者溶解度大,说明D的金属性强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氟化硼是平面正三角形,因此是非极性分子,推断三氯甲烷(碳原子位于分子结构中心)的结构和分子的极性情况是( )
A. 四面体,极性分子 B. 平面三角形,非极性分子
C. 正四面体,非极性分子 D. 平面三角形,极性分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质(括号内为杂质)的分离提纯方法错误的是( )
A. 溴苯(溴):氢氧化钠,分液 B. 乙酸乙酯(乙酸):氢氧化钠,分液
C. 乙醇(水):新制生石灰,蒸馏 D. 甲烷(乙烯):溴水,洗气
查看答案和解析>>
科目:高中化学 来源: 题型:
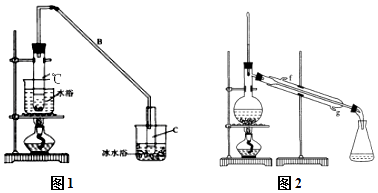
【题目】某化学小组采用类似制乙酸乙酯的装置(如图1),以环己醇制备环己烯 已知: 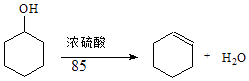
密度(g/cm3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
环己醇 | 0.96 | 25 | 161 | 能溶于水 |
环己烯 | 0.81 | ﹣103 | 83 | 难溶于水 |
(1)制备粗品:将12.5mL环己醇加入试管A中,再加入1mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品. ①A中碎瓷片的作用是 , 导管B除了导气外还具有的作用是 .
②试管C置于冰水浴中的目的是 .
(2)制备精品: ①环己烯粗品中含有环己醇和少量酸性杂质等.加入饱和食盐水,振荡、静置、分层,环己烯在 层(填上或下),分液后,用(填编号)洗涤环己烯.
A.KMnO4溶液 B.稀H2SO4 C.Na2CO3溶液 D.NaOH溶液
②再将环己烯按图2装置蒸馏,冷却水从(填f或g)口进入,蒸馏时要加入生石灰,目的是 .
③收集产品时,控制的温度应在 左右,实验制得的环己烯精品质量低于理论产量,可能的原因是 .
A.蒸馏时从70℃开始收集产品 B.环己醇实际用量多了 C.制备粗品时环己醇随产品一起蒸出
(3)以下区分环己烯精品和粗品的方法,最简单的方法是 .
A.酸性KMnO4溶液
B.用金属钠
C.测定沸点
D.溴的四氯化碳溶液.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是一个化学过程的示意图.请回答下列问题: 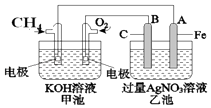
(1)甲池是装置(填“原电池”或“电解池”),B(石墨)电极的名称 是 .
(2)写出电极反应式: 通入CH4的电极;A(Fe)电极 .
(3)甲池中反应的离子方程式为 .
(4)乙池中反应的化学方程式为 .
(5)若乙池溶液体积为500mL,且忽略电解过程中溶液体积的变化,当乙池中 A极的质量增加5.40g时: ①甲池中理论上消耗O2体积为(标准状况下);
②乙池中所得溶液的pH= .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com