
ЁОЬтФПЁПдк25ЁцЪБЃЌУмБеШнЦїжаXЁЂYЁЂZШ§жжЦјЬхЕФГѕЪМХЈЖШКЭЦНКтХЈЖШШчЯТБэЃК
ЮяжЪ | X | Y | Z |
ГѕЪМХЈЖШ/( molЁЄL1) | 0.1 | 0.2 | 0 |
ЦНКтХЈЖШ/( molЁЄL1) | 0.05 | 0.05 | 0.1 |
ЯТСаЫЕЗЈе§ШЗЕФЪЧ
AЃЎЗДгІДяЕНЦНКтЪБЃЌXКЭYЕФзЊЛЏТЪЯрЕШ
BЃЎдіДѓбЙЧПЪЙЦНКтЯђЩњГЩZЕФЗНЯђвЦЖЏЃЌЦНКтГЃЪ§діДѓ
CЃЎЗДгІПЩБэЪОЮЊX+3Y![]() 2ZЃЌЦфЦНКтГЃЪ§ЮЊ1600
2ZЃЌЦфЦНКтГЃЪ§ЮЊ1600
DЃЎШєИУЗДгІЕФе§ЗДгІЗНЯђЮЊЗХШШЗДгІЃЌЩ§ИпЮТЖШЃЌЛЏбЇЗДгІЫйТЪдіДѓЃЌЗДгІЕФЦНКтГЃЪ§вВдіДѓ
ЁОД№АИЁПC
ЁОНтЮіЁПгЩЭМБэЪ§ОнПЩвдМЦЫуЃЌXЕФзЊЛЏТЪЮЊ(0.05 molЁЄL1/0.1 molЁЄL1)ЁС100%=50%ЃЌYЕФзЊЛЏТЪЮЊ (0.15 molЁЄL1/0.2 molЁЄL1)ЁС100%=75%ЃЌ AДэЮѓЃЛЖдгквЛИіПЩФцЗДгІЃЌЦНКтГЃЪ§гыХЈЖШЁЂбЙЧПКЭДпЛЏМСЮоЙиЃЌжЛгыЮТЖШгаЙиЃЌЙЪBДэЮѓЃЛЭМБэжаXЁЂYЁЂZЕФБфЛЏСПвРДЮЮЊ0.05 molЁЄL1ЁЂ0.15 molЁЄL1ЁЂ0.1 molЁЄL1ЃЌЦфХЈЖШБфЛЏБШЮЊ1ЃК3ЃК2ЃЌМДЛЏбЇМЦСПЪ§жЎБШЮЊ1ЃК3ЃК2ЃЌЙЪИУЗДгІПЩБэЪОЮЊX+3Y![]() 2ZЃЌНЋБэжаЦНКтЪБИїЮяжЪЕФХЈЖШДњШыЦНКтГЃЪ§БэДяЪНМЦЫуЃЌ
2ZЃЌНЋБэжаЦНКтЪБИїЮяжЪЕФХЈЖШДњШыЦНКтГЃЪ§БэДяЪНМЦЫуЃЌ![]() =1600ЃЌCе§ШЗЃЛгЩгкИУЗДгІЕФе§ЗДгІЗНЯђЮЊЗХШШЗДгІЃЌвђДЫЃЌЩ§ѓ{ЮТЖШЃЌЛЏбЇЦНКтЯђФцЗДгІЗНЯђвЦЖЏЃЌЦНКтГЃЪ§МѕаЁЃЌDДэЮѓЁЃ
=1600ЃЌCе§ШЗЃЛгЩгкИУЗДгІЕФе§ЗДгІЗНЯђЮЊЗХШШЗДгІЃЌвђДЫЃЌЩ§ѓ{ЮТЖШЃЌЛЏбЇЦНКтЯђФцЗДгІЗНЯђвЦЖЏЃЌЦНКтГЃЪ§МѕаЁЃЌDДэЮѓЁЃ



| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПєЧЛљБтЬвЫсЪЧвЉЮяКЯГЩЕФживЊжаМфЬхЃЌЫќПЩгЩБНЗгКЭввШЉЫсЗДгІжЦЕУЃЎ ЯТСагаЙиЫЕЗЈе§ШЗЕФЪЧЃЈ ЃЉ 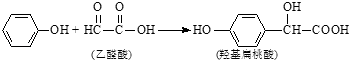
A.БНЗгКЭєЧЛљБтЬвЫсЛЅЮЊЭЌЯЕЮя
B.ГЃЮТЯТЃЌ1molєЧЛљБтЬвЫсжЛФмгы1mol Br2ЗДгІ
C.ввШЉЫсЕФКЫДХЙВеёЧтЦзжажЛга1ИіЮќЪеЗх
D.єЧЛљБтЬвЫсПЩвдЗЂЩњШЁДњЁЂбѕЛЏЁЂМгГЩЕШЗДгІ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЪвЮТЬѕМўЯТЃЌЯТСагаЙиЕчНтжЪШмвКЕФУшЪіе§ШЗЕФЪЧЃЈ ЃЉ
A.ЯђNa2CO3ШмвКжаЭЈШыCO2жСШмвКЮЊжаадЃЌдђ ![]() ЃО1
ЃО1
B.pHЯрЭЌЕФАБЫЎКЭBa ЃЈOHЃЉ2ШмвКжаЃК2c ЃЈNH4+ЃЉ=c ЃЈ Ba2+ЃЉ
C.ЕШХЈЖШЕФKHSO3ШмвКгыKOHШмвКЕШЬхЛ§ЛьКЯЃКcЃЈOHЉЃЉЉcЃЈH+ЃЉ=cЃЈHSO3ЉЃЉ+cЃЈH2SO3ЃЉ
D.ЯђMg ЃЈOHЃЉ2зЧвКжаМгШыЩйСПNH4ClЗлФЉ ![]() ВЛБф
ВЛБф
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЁАцЯЖ№БМдТЁБЪЧвЛИіГфТњРЫТўжївхЕФжаЙњЩёЛАЙЪЪТЃЎ2007Фъ10дТ24ШеЮвЙњЁАцЯЖ№вЛКХЁБЬНдТЮРаЧгЩГЄШ§МзЛ№М§ЫЭШыдЄЖЈЕФЙьЕРЃЎГЄШ§МзЛ№М§ЕкШ§МЖЭЦНјМСВЩгУЕЭЮТвКбѕ/вКЧтЃЎвбжЊдк298KЪБЃЌ2gЧтЦјгыбѕЦјЭъШЋЗДгІЩњГЩвКЬЌЫЎЗХШШ285.8kJЃЌдђДЫЗДгІЕФШШЛЏбЇЗНГЬЪНЮЊЃЈ ЃЉ
A.2H2ЃЈgЃЉ+O2ЃЈgЃЉЈT2H2OЃЈlЃЉЁїH=Љ285.8KJmolЉ1
B.2H2ЃЈgЃЉ+O2ЃЈgЃЉЈT2H2OЃЈlЃЉЁїH=+285.8KJmolЉ1
C.2H2ЃЈgЃЉ+O2ЃЈgЃЉЈT2H2OЃЈlЃЉЁїH=Љ571.6KJmolЉ1
D.2H2ЃЈgЃЉ+O2ЃЈgЃЉЈT2H2OЃЈlЃЉЁїH=+571.6KJmolЉ1
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПОнБЈЕРЃЌЮвЙњгЕгаЭъШЋзджїВњШЈЕФЧтбѕШМСЯЕчГиГЕНЋдкББОЉАТдЫЛсЦкМфЮЊдЫЖЏдБЬсЙЉЗўЮёЁЃФГжжЧтбѕШМСЯЕчГиЕФЕчНтжЪШмвКЮЊKOHШмвКЁЃЯТСагаЙиИУЕчГиЕФа№ЪіВЛе§ШЗЕФЪЧ
A. е§МЋЗДгІЪНЮЊЃКO2ЃЋ2H2OЃЋ4eЃЃН4OHЃ
B. ЙЄзївЛЖЮЪБМфКѓЃЌЕчНтжЪШмвКжаKOHЕФЮяжЪЕФСПВЛБф
C. ИУШМСЯЕчГиЕФзмЗДгІЗНГЬЪНЮЊЃК2H2ЃЋO2ЃН2H2O
D. гУИУЕчГиЕчНтCuCl2ШмвКЃЌВњЩњ2.24 L Cl2(БъзМзДПі)ЪБЃЌга0.1 molЕчзгзЊвЦ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаИїзщРызгвЛЖЈФмДѓСПЙВДцЕФЪЧ
A. дкЮоЩЋШмвКжаЃКNH4+ЁЂFe2+ЁЂSO42-ЁЂCO32-
B. дкКЌДѓСПBa2+ШмвКжаЃКNH4+ЁЂNa+ЁЂCl-ЁЂCO32-
C. дкЧПМюШмвКжаЃКNa+ЁЂK+ЁЂCl-ЁЂSO32-
D. дкЫсадЕФШмвКжаЃКK+ЁЂFe2+ЁЂCl-ЁЂCH3COO-
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПНЋЙЬЬхNH4IжУгкУмБеШнЦїжаЃЌдквЛЖЈЮТЖШЯТЗЂЩњЯТСаЗДгІЃКЂйNH4I(sЃЉ![]() NH3(gЃЉ+HI(gЃЉЃЛЂк2HI(g)
NH3(gЃЉ+HI(gЃЉЃЛЂк2HI(g)![]() H2(g)+I2(g)ЁЃДяЕНЦНКтЪБЃЌc(H2)=0.5 mol/LЃЌc(HI)=3 mol/LЃЌдђДЫЮТЖШЯТЗДгІЂйЕФЦНКтГЃЪ§ЮЊ
H2(g)+I2(g)ЁЃДяЕНЦНКтЪБЃЌc(H2)=0.5 mol/LЃЌc(HI)=3 mol/LЃЌдђДЫЮТЖШЯТЗДгІЂйЕФЦНКтГЃЪ§ЮЊ
AЃЎ9 BЃЎ16 CЃЎ12 DЃЎ25
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПНЋБэУцвбЭъШЋЖлЛЏЕФТСЬѕЃЌВхШыЯТСаШмвКжаЃЌВЛЛсЗЂЩњЗДгІЕФЪЧЃЈЁЁЁЁЃЉ
A.ЯЁЯѕЫсB.ЯѕЫсЭC.ЯЁбЮЫсD.ЧтбѕЛЏФЦ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЕчНтЗЈДІРэКЌЕЊбѕЛЏЮяЗЯЦјЃЌПЩЛиЪеЯѕЫсЃЌОпгаНЯИпЕФЛЗОГаЇвцКЭОМУаЇвцЃЎЪЕбщЪвФЃФтЕчНтЗЈЮќЪеNOxЕФзАжУШчЭМЫљЪОЃЈЭМжаЕчМЋОљЮЊЪЏФЋЕчМЋЃЉЃЎ 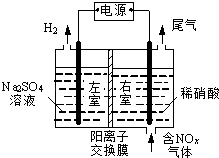
ЃЈ1ЃЉШєгУNO2ЦјЬхНјааФЃФтЕчНтЗЈЮќЪеЪЕбщЃЎ ЂйаДГіЕчНтЪБNO2ЗЂЩњЗДгІЕФЕчМЋЗДгІЪНЃК ЃЎ
ЂкШєгаБъзМзДПіЯТ2.24LNO2БЛЮќЪеЃЌЭЈЙ§бєРызгНЛЛЛФЄЃЈжЛдЪаэбєРызгЭЈЙ§ЃЉЕФH+ЮЊmolЃЎ
ЃЈ2ЃЉФГаЁзщдкгвЪвзАга10L0.2molLЉ1ЯѕЫсЃЌгУКЌNOКЭNO2ЃЈВЛПМТЧNO2зЊЛЏЮЊN2O4ЃЉЕФЗЯЦјНјааФЃФтЕчНтЗЈЮќЪеЪЕбщЃЎ ЂйЪЕбщЧАЃЌХфжЦ10L0.2molLЉ1ЯѕЫсШмвКашСПШЁmLЕФУмЖШЮЊ1.4gmLЉ1ЁЂжЪСПЗжЪ§ЮЊ63%ЕФХЈЯѕЫсЃЎ
ЃЈ3ЃЉЂкЕчНтЙ§ГЬжаЃЌгаВПЗжNOзЊЛЏЮЊHNO2 ЃЌ ЪЕбщНсЪјЪБЃЌВтЕУгвЪвШмвКжаКЌ3molHNO3ЁЂ0.1molHNO2 ЃЌ ЭЌЪБзѓЪвЪеМЏЕНБъзМзДПіЯТ28LH2 ЃЎ МЦЫудЦјЬхжаNOКЭNO2ЕФЬхЛ§БШЃЈМйЩшЮВЦјжаВЛКЌЕЊбѕЛЏЮяЃЌаДГіМЦЫуЙ§ГЬЃЉЃЎ
ВщПДД№АИКЭНтЮі>>
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com