
 X、Y、Z、W均为短周期元素,它们在元素周期表中相对位置如图所示,若Z原子的最外层电子数是第一层电子数的3倍,下列说法正确的是( )
X、Y、Z、W均为短周期元素,它们在元素周期表中相对位置如图所示,若Z原子的最外层电子数是第一层电子数的3倍,下列说法正确的是( )| A. | Z单质与氢气反应较Y剧烈 | |
| B. | 最高价氧化物对应水化物酸性W比Z强 | |
| C. | X单质氧化性强于Y单质 | |
| D. | X与W的原子核外电子数相差9 |
分析 X、Y、Z、W均为短周期元素,由元素相对位置可知,X和Y处于第二周期,Z和W处于第三周期,若Z原子的最外层电子数是第一层电子数的3倍,第一层电子为2,则Z元素最外层电子数是6,所以Z是S元素,可推知W为Cl元素,Y是O元素,X是N元素,结合元素周期律来分析解答.
解答 解:X、Y、Z、W均为短周期元素,由元素相对位置可知,X和Y处于第二周期,Z和W处于第三周期,若Z原子的最外层电子数是第一层电子数的3倍,第一层电子为2,则Z元素最外层电子数是6,所以Z是S元素,可推知W为Cl元素,Y是O元素,X是N元素.
A.非金属性Y(O)>Z(S),所以Y的单质与氢气反应较Z剧烈,故A错误;
B.非金属性W(Cl)>Z(S),所以最高价氧化物对应水化物的酸性W比Z强,故B正确;
C.X为N元素、Y为O元素,氧元素非金属性较强,故氮气的氧化性小于氧气,故C错误;
D.X为N元素、W为Cl元素,二者原子序数相差17-7=10,故D错误,
故选B.
点评 本题考查位置结构性质的应用,Z为解答本题的突破口,注意对元素周期律的理解掌握,题目难度不大.


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:解答题
| 物质 | 摩尔质量g/mol-1 | 密度 | 1mol物质的体积 |
| Al | 26.98 | 2.70g•cm-3 | |
| Fe | 55.85 | 7.86g•cm-3 | |
| H2O | 18.02 | 0.998g•cm-3 | |
| C2H5OH | 46.07 | 0.789g•cm-3 | |
| H2 | 2.016 | 0.0899g•L-1 | |
| N2 | 28.02 | 1.25g•L-1 | |
| CO | 28.01 | 1.25g•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
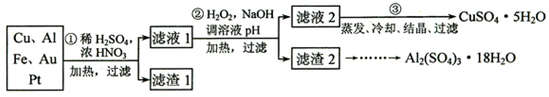
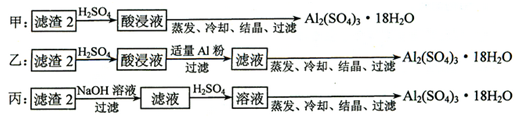
查看答案和解析>>
科目:高中化学 来源: 题型:填空题


查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 反应温度/℃ | 反应时间(min) | 收率 |
| 30~35 | 180 | 10.0 |
| 20~25 | 60 | 18.0 |
| 20~25 | 120 | 26.0 |
| 20~25 | 180 | 58.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ①③ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增加N2的量,可以加快反应速率 | |
| B. | 当N2和H2全部转化为NH3时,反应才达到最大限度 | |
| C. | 达到平衡时,H2和NH3的浓度比一定为3:2 | |
| D. | 分别用N2和NH3来表示该反应的速率时,数值大小相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢化物稳定性:Y>Z | |
| B. | XW3与WZ相遇,产生大量白烟 | |
| C. | 氧化物的水化物的酸性:Y<Z | |
| D. | X与Z不能同时存在于同一离子化合物中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 推广使用燃煤脱硫技术,在燃煤中加入适量石灰石,可减少废气中的SO2 | |
| B. | 实施绿化工程,防治扬尘污染 | |
| C. | 研制开发燃料电池汽车,消除机动车尾气污染 | |
| D. | 加高工厂的烟囱,使烟尘和废气远离地表 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com