
 非极性 (2) [ Cr(H2O)5 Cl ]2+
非极性 (2) [ Cr(H2O)5 Cl ]2+ 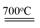 3CH4+GaAs (4)三角锥形 sp2 (5) 3
3CH4+GaAs (4)三角锥形 sp2 (5) 3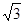 · b/16a3NA
· b/16a3NA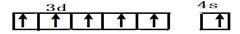 。因为CrO2Cl2常温下为深红色液体,能与CCl4、CS2等互溶。根据相似相容原理,可判断出CrO2Cl2是非极性分子。(2) 浅绿色固体CrCl3·6H2O与足量硝酸银反应时,1mol固体可生成2mol氯化银沉淀,说明三个Cl-中只有一个作配位体,由于其配位数为6,所以还有5个水作配位体。则这种浅绿色固体中阳离子的化学式[ Cr(H2O)5 Cl ]2+。Ⅱ.(3)由题意得方程式:CH3)3Ga+AsH3
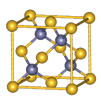
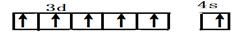
。因为CrO2Cl2常温下为深红色液体,能与CCl4、CS2等互溶。根据相似相容原理,可判断出CrO2Cl2是非极性分子。(2) 浅绿色固体CrCl3·6H2O与足量硝酸银反应时,1mol固体可生成2mol氯化银沉淀,说明三个Cl-中只有一个作配位体,由于其配位数为6,所以还有5个水作配位体。则这种浅绿色固体中阳离子的化学式[ Cr(H2O)5 Cl ]2+。Ⅱ.(3)由题意得方程式:CH3)3Ga+AsH3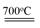 3CH4+GaAs。(4)同族元素形成的化合物结构相似。NH3为三角锥形,所以AsH3空间构型为三角锥形。因为(CH3)3Ga为非极性分子,说明这几个化学键是对称的。故其中镓原子的杂化方式是sp2杂化。(5)在砷化镓晶胞中,含有Ga:8×1/8+6×1/2=4,含有As:4个,因此每个晶胞中含有4和GaAs。在砷化镓晶体中最近的砷和镓原子核间距为a cm,由于As处于与它相连的四个Ga构成的四面体的几何中心。距离最近且相等的As原子之间的距离为L.则
3CH4+GaAs。(4)同族元素形成的化合物结构相似。NH3为三角锥形,所以AsH3空间构型为三角锥形。因为(CH3)3Ga为非极性分子,说明这几个化学键是对称的。故其中镓原子的杂化方式是sp2杂化。(5)在砷化镓晶胞中,含有Ga:8×1/8+6×1/2=4,含有As:4个,因此每个晶胞中含有4和GaAs。在砷化镓晶体中最近的砷和镓原子核间距为a cm,由于As处于与它相连的四个Ga构成的四面体的几何中心。距离最近且相等的As原子之间的距离为L.则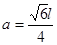 ;
; .最近的两个As在晶胞面对角线的1/2处。设该晶胞的长度是x,则
.最近的两个As在晶胞面对角线的1/2处。设该晶胞的长度是x,则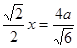 ;解得x=
;解得x=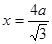 是则砷化镓晶体密度的表达式为:
是则砷化镓晶体密度的表达式为: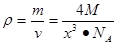 .整理可得
.整理可得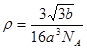 。
。

 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科目:高中化学 来源:不详 题型:填空题
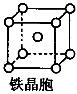
 3Na2O+2Fe+9N2↑。
3Na2O+2Fe+9N2↑。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.主族元素的原子核外电子最后填入的能级是d能级或f能级 |
| B.镁型和铜型金属晶体的配位数均为12 |
| C.中心原子上的孤电子对不参与决定分子的空间结构 |
| D.分子中键角越大,价电子对相互排斥力越大,分子越稳定 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
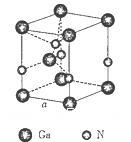
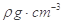 。列出计算氮化镓晶胞边长a的表达式:a=_______cm。
。列出计算氮化镓晶胞边长a的表达式:a=_______cm。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.相同类型的离子晶体,晶格能越大,形成的晶体越稳定 |
| B.手性催化剂只催化或者主要催化一种手性分子的合成 |
| C.用金属的电子气理论能合理地解释金属易腐蚀的原因 |
| D.H3O+、NH4Cl和[Ag(NH3)2]+中均存在配位键 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.离子键 | B.共价键 | C.金属键 | D.配位键 E.氢键 F. 键 键 |

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
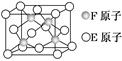
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
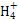 立体构型是 ,其中心原子的杂化方式为 。
立体构型是 ,其中心原子的杂化方式为 。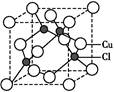
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.依据元素的原子序数,推断该元素原子的核外电子数 |
| B.依据原子最外层电子数的多少,推断元素金属性、非金属性的强弱 |
| C.依据气体的摩尔质量,推断相同状态下不同气体密度的大小 |
| D.依据液体物质的沸点,推断将两种互溶液态混合物用蒸馏法分离的可行性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com