
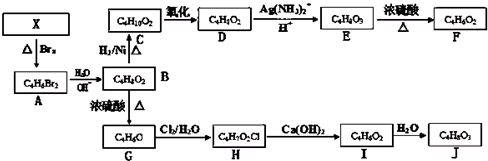
 .再分析另一条线,由B与G的分子式可知,B脱去1分子水生成G,系列转化得到I可以发生水解反应生成J,则B→G应该是分子内成醚,故G为
.再分析另一条线,由B与G的分子式可知,B脱去1分子水生成G,系列转化得到I可以发生水解反应生成J,则B→G应该是分子内成醚,故G为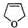 ;G→H应该是G与HClO发生加成反应,H应该为
;G→H应该是G与HClO发生加成反应,H应该为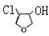 ;H→I是:2
;H→I是:2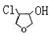 +Ca(OH)2=2
+Ca(OH)2=2 +CaCl2+2 H2O;I→J是醚的开环,五元环相对于三元环稳定,因此反应为
+CaCl2+2 H2O;I→J是醚的开环,五元环相对于三元环稳定,因此反应为 .
. .再分析另一条线,由B与G的分子式可知,B脱去1分子水生成G,系列转化得到I可以发生水解反应生成J,则B→G应该是分子内成醚,故G为
.再分析另一条线,由B与G的分子式可知,B脱去1分子水生成G,系列转化得到I可以发生水解反应生成J,则B→G应该是分子内成醚,故G为 ;G→H应该是G与HClO发生加成反应,H应该为
;G→H应该是G与HClO发生加成反应,H应该为 ;H→I是:2
;H→I是:2 +Ca(OH)2=2
+Ca(OH)2=2 +CaCl2+2 H2O;I→J是醚的开环,五元环相对于三元环稳定,因此反应为
+CaCl2+2 H2O;I→J是醚的开环,五元环相对于三元环稳定,因此反应为 ,
, ,E发生分子内酯化反应生成F,反应方程式为:HOCH2CH2CH2COOH
,E发生分子内酯化反应生成F,反应方程式为:HOCH2CH2CH2COOH| 浓硫酸 |
| △ |
 +H2O;
+H2O;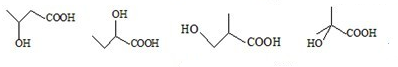 ,
,| 浓硫酸 |
| △ |
 +H2O;
+H2O; ;
; ,故答案为:
,故答案为: ;
; ,故答案为:
,故答案为: .
.


科目:高中化学 来源: 题型:
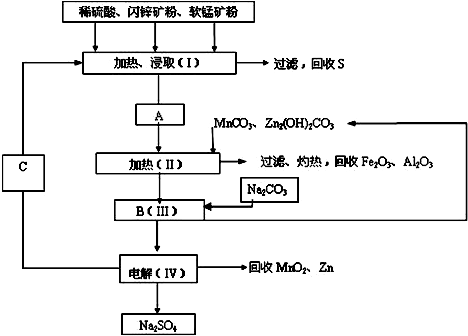
查看答案和解析>>
科目:高中化学 来源: 题型:
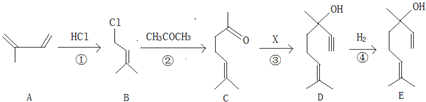
查看答案和解析>>
科目:高中化学 来源: 题型:
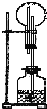
| A、块状大理石和稀硫酸 |
| B、NH4Cl与稀NaOH溶液 |
| C、Na2O2与NaOH溶液 |
| D、铜片与稀盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1mol的白磷(P4)或四氯化碳(CCl4)中所含的共价键数均为0.4NA |
| B、1L amol/L的氯化铁溶液中,若Fe3+的数目为NA,则Cl-的数目为3NA |
| C、0.1 molN2和0.3molH2在一定条件下充分反应,转移电子数目为0.6NA |
| D、常温常压下,65gZn与足量浓 H2SO4充分反应,转移电子数一定为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
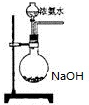 氨在国民经济中占有重要地位.
氨在国民经济中占有重要地位.查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/(mol?L-1) | 0.64 | 0.50 | 0.50 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com