
 .
. 分析 反应中KClO3+6HCl=KCl+3Cl2↑+3H2O中,只有Cl元素化合价发生变化,当有3mol Cl2生成时,转移5mol电子,据此分析解答.
解答 解:反应KClO3+6HCl=KCl+3Cl2↑+3H2O中,氯气、水在离子反应中保留化学式,则该反应的离子反应为ClO3-+5Cl-+6H+=3Cl2↑+3H2O,
反应KClO3+6HCl=KCl+3Cl2↑+3H2O中,只有Cl元素化合价发生变化,当有3mol Cl2生成时,转移5mol电子,则电子转移的方向和数目为 ,故答案为:ClO3-+5Cl-+6H+=3Cl2↑+3H2O;
,故答案为:ClO3-+5Cl-+6H+=3Cl2↑+3H2O; .
.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念及转移电子的考查,题目难度不大.


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:选择题
| A. | 容器内每减少1mol I2,同时生成2mol HI | |
| B. | 容器内气体压强不再变化 | |
| C. | 混合气体的颜色不再变化 | |
| D. | 混合气体的密度恒定不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
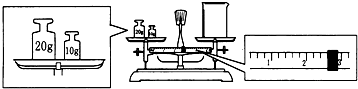
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增加C的量 | B. | 将容器的体积缩小一半 | ||
| C. | 保持体积不变,充入N2 | D. | 压强不变充入N2使体积增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | Cl2+2KBr═Br2+2KCl | B. | 2NaHCO3═Na2CO3+H2O+CO2↑ | ||
| C. | 4Fe(OH)2+O2+2H2O═4Fe(OH)3 | D. | 2K2O2+2CO2═2K2CO3+O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 71g Cl2所含的原子数为2NA | |
| B. | 18g水中所含电子数为10 NA | |
| C. | 24g Mg与足量的盐酸反应转移电子数为 NA | |
| D. | 在1L 2mol/L的硝酸镁溶液中含有的硝酸根离子数为4 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
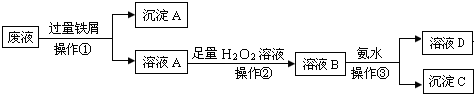
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com