
| A. | Zn+H2SO4=ZnSO4+H2↑ | B. | 2KClO3$→_{△}^{MnO_{2}}$ 2KCl+3O2↑ | ||
| C. | CaO+H2O=Ca(OH)2 | D. | H2+Cl2$\frac{\underline{\;点燃\;}}{\;}$ 2HCl |
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案科目:高中化学 来源: 题型:解答题
| 实验编号 | ① | ② | ③ |
| 盐酸体积 | 50mL盐酸 | 50mL盐酸 | 50mL盐酸 |
| m(混合物) | 9.2g | 16.56g | 27.6g |
| V(CO2)(标况) | 2.24L | 3.36L | 3.36L |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 9 min | B. | 27 min | C. | 13.5 min | D. | 3 min |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 在恒温恒容条件下,将一定量NO2和N2O4的混合气体通入容积为2L的密闭容器中发生反应:N2O4(g)?2NO2(g)△H>0,反应过程中各物质的物质的量浓度(c)随时间(t)的变化曲线如图所示.
在恒温恒容条件下,将一定量NO2和N2O4的混合气体通入容积为2L的密闭容器中发生反应:N2O4(g)?2NO2(g)△H>0,反应过程中各物质的物质的量浓度(c)随时间(t)的变化曲线如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 汞合金是一种具有金属特性的物质 | B. | 汞合金的强度和硬度比锡的大 | ||
| C. | 汞合金的熔点比汞的低 | D. | 汞合金的毒性远低于汞的毒性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ②④ | C. | ③④⑤ | D. | ①③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝土矿中的铝元素是以化合态存在的,需用化学方法把铝元素变成游离态 | |
| B. | 提炼过程中,先将铝土矿净化提取氧化铝,再进行冶炼 | |
| C. | 可用常见的还原剂把氧化铝中的铝还原出来 | |
| D. | 冶炼铝的方法与工业冶炼钠、镁相似,可用电解法 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
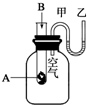 为了研究化学反应A+B=C+D的能量变化,某同学设计了如图所示装置.当向盛有A的试管中滴加试剂B时,看到U形管中甲处液面下降乙处液面上升.试回答下列问题:
为了研究化学反应A+B=C+D的能量变化,某同学设计了如图所示装置.当向盛有A的试管中滴加试剂B时,看到U形管中甲处液面下降乙处液面上升.试回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com