
【题目】分子式为C4H10O并能与金属钠反应放出氢气的有机化合物有(不含立体异构)
A.3种 B.4种 C.5种 D.6种
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】(8分) 研究NO2、SO2、CO等大气污染气体的处理具有重要意义。
(1)对于反应:2SO2(g)+O2(g)![]() 2SO3(g);如果反应速率υ(SO2)为0.05 mol·L-1·min-1,则υ(O2)= ;υ(SO3)= 。
2SO3(g);如果反应速率υ(SO2)为0.05 mol·L-1·min-1,则υ(O2)= ;υ(SO3)= 。
(2)已知:2SO2(g)+O2(g) ![]() 2SO3(g) ΔH=-196.6 kJ·mol-1
2SO3(g) ΔH=-196.6 kJ·mol-1
2NO(g)+O2(g) ![]() 2NO2(g) ΔH=-113.0 kJ·mol-1
2NO2(g) ΔH=-113.0 kJ·mol-1
则反应NO2(g)+SO2(g) ![]() SO3(g)+NO(g)的ΔH=______ kJ·mol-1。
SO3(g)+NO(g)的ΔH=______ kJ·mol-1。
(3)一定条件下,将NO2与SO2以体积比1∶2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是______。
a、体系压强保持不变 b、混合气体颜色保持不变
c、SO3和NO的体积比保持不变 d、每消耗1 mol SO3的同时生成1 mol NO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学在试管中做铁钉与稀硫酸反应的实验,发现反应速率较慢,下列措施:①给试管加热 ②加入铁粉 ③加入冰块④加入少量醋酸钠晶体 ⑤将稀硫酸换为浓硫酸,能加快反应速率的是
A.①②⑤ B.①② C.③④ D.③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】重铬酸钾是一种常见的强氧化剂。实验室以精选铬铁矿(主要成分可表示为FeO.Cr2O3,还含有SiO2、Al2O3等杂质)为原料制备重铬酸钾晶体(K2Cr2O7,式量294)的流程如下:

请回答下列问题:
(1)操作1中发生的反应有:
4FeO·Cr2O3 + 8Na2CO3 + 7O2 = 8Na2CrO4 + 2Fe2O3 + 8CO2↑
Na2CO3 + Al2O3 = 2NaAlO2 + CO2↑ Na2CO3 + SiO2 = Na2SiO3 + CO2↑
该步骤在常温下的反应速率较慢,为使反应速率增大,可采取的措施是_____________________,__________________________。(写出两条)
(2)固体Y中主要含有 ______________。(填写化学式)
(3)酸化步骤使含铬物质发生了转化为_________,请写出离子反应方程式____________。
(4)操作4中的化学反应在溶液中能发生的可能理由是_________________,获得晶体的操作依次是:加入KCl固体,在水浴上加热浓缩至____________________,冷却结晶,抽滤、洗涤、干燥。
(5)通过下列实验可测定产品中重铬酸钾的质量分数:
称取重铬酸钾试样1.470g,用100mL容量瓶配制成溶液。移取25.00mL溶液于碘量瓶中,加入适量稀硫酸和足量碘化钾(铬的还原产物为Cr3+),放于暗处5min。然后加入一定量的水,加入淀粉指示剂,用0.1500mol/L Na2S2O3标准溶液滴定,共消耗标准液36.00mL。滴定时发生的反应的离子方程式为:I2 + 2S2O32- = 2I- + S4O62-则所测定产品中重铬酸钾的纯度为___________。
(6)有关上述实验过程中涉及的部分实验操作的描述,正确的是____________。
A.粗产品若要进一步提纯,可以采用重结晶的方法
B.配制溶液时,用托盘天平称取试样后,一般经溶解、转移(含洗涤)、定容等步骤,配制成100mL溶液
C.滴定时,当最后一滴标准溶液滴入时,溶液变为蓝色,且半分钟内不变色,可判断滴定终点
D.滴定终点时俯视读数,测定结果偏低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳、硫和氮元素及其化合物的处理,是资源利用和环境保护的重要研究课题。
⑴CO可转化成二甲醚,原理为:2CO(g) + 4H2(g) ![]() CH3OCH3(g) + H2O(g),已知一定条件下,该反应中CO的平衡转化率随温度、投料比的变化曲线如下图左所示,若温度升高,则反应的平衡常数K将 (填“增大”、“减小”或“不变”)
CH3OCH3(g) + H2O(g),已知一定条件下,该反应中CO的平衡转化率随温度、投料比的变化曲线如下图左所示,若温度升高,则反应的平衡常数K将 (填“增大”、“减小”或“不变”)

⑵SO2的水溶液呈酸性,某温度下,0.02mol/L亚硫酸水溶液的pH等于2,若忽略亚硫酸的二级电离和H2O的电离,则该温度下亚硫酸的一级电离平衡常数Ka1= 。
⑶已知:反应1 2SO2(g) + O2(g) ![]() 2SO3(g) ΔH1
2SO3(g) ΔH1
反应2 2NO(g) + O2(g) ![]() 2NO2(g) ΔH2
2NO2(g) ΔH2
若ΔH1 <ΔH2 < 0,则反应3 SO2(g) + NO2(g) ![]() SO3(g) + NO(g) 属于 (填“放热”或“吸热”)反应。
SO3(g) + NO(g) 属于 (填“放热”或“吸热”)反应。
⑷若用少量NaOH溶液吸收SO2气体,对产物NaHSO3进一步电解可制得硫酸,电解原理示意图(见上图右所示),则电解时阳极的电极反应式为 。
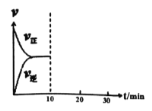
⑸在恒温密闭容器中通入SO2和NO2各1mol发生反应3:SO2(g) + NO2(g) ![]() SO3(g) + NO(g),当反应达到平衡后(此时NO2的转化率为α1),维持温度和容积不变,10min时再通入各1mol的SO2和NO2的混合气体,20min时再次平衡(此时NO2的转化率为α2)。两次平衡时NO2的转化率α1 α2(填“>”、“<”、“=”),并在下图中画出正反应速率在10-30min间随时间变化的曲线图。
SO3(g) + NO(g),当反应达到平衡后(此时NO2的转化率为α1),维持温度和容积不变,10min时再通入各1mol的SO2和NO2的混合气体,20min时再次平衡(此时NO2的转化率为α2)。两次平衡时NO2的转化率α1 α2(填“>”、“<”、“=”),并在下图中画出正反应速率在10-30min间随时间变化的曲线图。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把一块镁铝合金投入到1 mol ·L-1 HC1溶液里,待合金完全溶解后,再往溶液里加入 1 mol L-1 NaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积变化的关系如右图所示。下列说法中错误的是( )
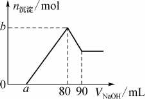
A.HC1溶液的体积为80 mL B.a的取值范围为0≤a<50
C.当a值为30时,b值为0.01 D.当a值为10时,b值为0.03
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,属于氧化还原反应的是( )
A.2 Al(OH)3![]() Al2O3+3 H2O
Al2O3+3 H2O
B.2H2O2![]() 2H2O+O2↑
2H2O+O2↑
C.FeO+2 HCl═FeCl2+H2O
D.FeCl2+2NaOH═Fe (OH)2↓+2NaCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设![]() 为阿伏加德罗常数的值,下列说法正确的是( )
为阿伏加德罗常数的值,下列说法正确的是( )
A.常温常压下,7.8g Na2S和Na2O2的混合物中,阴离子所含电子数为1.8![]()
B.标准状况下,11.2LSO3中含有的分子数目为0.5 ![]()
C.常温常压下,46gNO2与 N2O4的混合气体含有的氮原子数目无法计算
D.0.1 mo1 L-1 MgC12溶液中含有的Mg2+数目小于0.1 ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示为氢氧燃料电池的原理示意图,按照此图的提示,下列叙述不正确的是( )
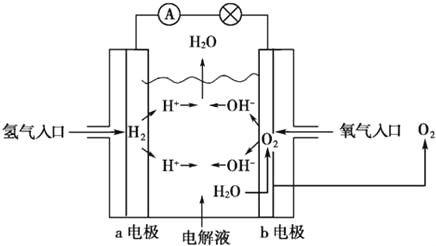
A.a电极是负极
B.b电极的电极反应为:4OH﹣﹣4e﹣═2H2O+O2↑
C.氢氧燃料电池是一种具有应用前景的绿色电源
D.氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com