
| A. | CS2 | B. | H2S | C. | SO2 | D. | SO3 |
分析 根据价层电子对互斥理论确定中心原子杂化类型,价层电子对个数=σ键个数+孤电子对个数,σ键个数=配原子个数,孤电子对个数=$\frac{1}{2}$(a-xb),a指中心原子价电子个数,x指配原子个数,b指配原子形成稳定结构需要的电子个数;正负电荷重心重合的分子是非极性分子,否则是极性分子,据此分析解答.
解答 解:A.二硫化碳中C原子价层电子对个数=2+$\frac{1}{2}$×(4-2×2)=2,所以采用sp杂化,该分子为直线形分子,正负电荷重心重合,为非极性分子,故A错误;
B.硫化氢分子中S原子价层电子对个数=2+$\frac{1}{2}$×(6-1×2)=4,所以采用sp3杂化,为V形结构,正负电荷重心不重合,为极性分子,故B错误;
C.二氧化硫分子中S原子价层电子对个数=2+$\frac{1}{2}$×(6-2×2)=3,所以采用sp2杂化,含有一个孤电子对,为V形结构,正负电荷重心不重合,为极性分子,故C错误;
D.三氧化硫分子中S原子价层电子对个数=3+$\frac{1}{2}$×(6-3×2)=3,所以采用sp2杂化,为平面正三角形结构,正负电荷重心重合,为非极性分子,故D正确;
故选D.
点评 本题考查原子杂化方式判断、分子空间构型判断、分子极性判断,为高频考点,明确价层电子对互斥理论即可解答,注意孤电子对个数的计算方法,题目难度不大.


 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源: 题型:选择题
| A. | 沸点:戊烷>2,2一二甲基戊烷>2,3一二甲基丁烷>丙烷 | |
| B. | 密度:CCl4>CHCl3>H2O>苯 | |
| C. | 等物质的量的物质完全燃烧时耗O2量:乙烷>乙烯>甲烷 | |
| D. | 等质量的物质完全燃烧时耗O2量:甲烷>乙烷>乙烯>乙炔 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H4O和C3H6O均满足饱和一元醛的通式,因此它们一定互为同系物 | |
| B. | 乙烯和苯均可使溴水褪色,但是其褪色原理不同 | |
| C. | 乙烯和苯分子中各原子都在同一平面 | |
| D. | 检验乙烷中是否含有乙烯,试剂为酸性高锰酸钾溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
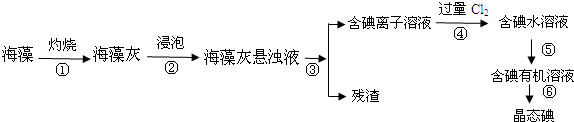
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 烃CnH2n+2 | B. | 醇CnH2n+2O | C. | 醛CnH2nO | D. | 羧酸CnH2nO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 其他条件不变,改变反应物的量,△H发生改变 | |
| B. | 上述反应生成1mol SO3,放热少于98.5KJ | |
| C. | 相同条件下加入2molSO2(g)、1mol O2(g) 充分反应放热等于197KJ | |
| D. | 相同条件下加入1molSO2(g)、0.5mol O2(g) 充分反应放热为Q1 kJ,若在相同容器中加入1mol SO3充分反应吸热等于Q2kJ,Q1kJ+Q2 kJ=98.5kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯酚钠溶液中通入少量CO2:2C6H5O-+CO2+H2O→2C6H5OH+CO32- | |
| B. | FeSO4的酸性溶液中加H2O2:2Fe2++H2O2+2H+═2Fe3++2H2O | |
| C. | 用氨水吸收少量的SO2:NH3•H2O+SO2═NH4++HSO3- | |
| D. | 碳酸氢钠溶液中加入过量石灰水:HCO3-+OH-═CO32-+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com