
(10分)
锂被誉为“高能金属”。工业上用硫酸与β-锂辉矿(LiAlSi2O6和少量钙镁杂质)在250~300℃反应,生成Li2SO4以及硅铝化合物、MgSO4等,其工业生产流程如下:

(1)用氧化物形式表示LiAlSi2O6的组成:___________________。
(2)沉淀X的主要成分是(写化学式)________________________。
(3)流程中两次使用了Na2CO3溶液,试说明前后浓度不同的原因:
____________________________________________________________________。
(4)锂和氢气在加热时能反应生成白色固体氢化锂,氢化锂遇到水就立即溶解并释放出大量的气体。试写出氢化锂遇水反应的化学方程式:_______________________________________。
(5)将盐酸与Li2C03完全反应后的溶液,加热蒸干得到固体,再将其熔融电解生产锂。电解时产生的氯气中会混有少量氧气,原因是____________________________________________。
科目:高中化学 来源: 题型:
(共8分)锂在原子能工业中具有十分独特的地位,被誉为“高能金属”,它推动着能源工业,尤其是电池技术的发展。盐湖卤水中锂的含量较高,资源丰富,提炼锂的价格低廉,成为国内外开发生产锂的主攻方向。把盐湖卤水自然日晒和冷冻,从卤水中析出食盐、泻利盐、钾盐镁矾和光卤石等一系列盐类,得到富含MgC12的浓缩母液,其中LiC1的浓度达10%以上。把浓缩母液经高温炉分解除去MgC12等一系列过程,最终得到金属锂。其主要生产工艺流程如下:
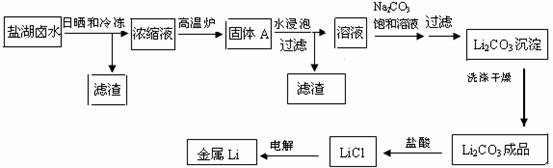 已知:Li2CO3在不同温度的溶解度如下表:
已知:Li2CO3在不同温度的溶解度如下表:
| 温度/℃ | 0 | 10 | 20 | 50 | 75 | 100 |
| Li2CO3的溶解度/g | 1.539 | 1.406 | 1.329 | 1.181 | 0.866 | 0.728 |
(1)写出浓缩母液在高温炉中分解的化学方程式
(2)写出盐酸与Li2CO3反应的离子方程式
(3)洗涤所得Li2CO3沉淀要用热水而非冷水,原因是 。
(4)熔融LiCl电解的环境是
a.氢气中b.氮气中c.空气中d.真空中e.He气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com