
”¾ĢāÄæ”æ½öÄÜŌŚĖ®ČÜŅŗĄļµ¼µēµÄµē½āÖŹŹĒ
A.NaOHB.SO2C.H2SO4D.BaSO4
”¾“š°ø”æC
”¾½āĪö”æ
A£®NaOHŌŚĖ®ČÜŅŗÖŠ»ņČŪȌדĢ¬ĻĀ¶¼Äܹ»µ¼µē£¬ŹĒµē½āÖŹ£¬Ń”ĻīA“ķĪó£»
B£®¶žŃõ»ÆĮņÖ»“ęŌŚ·Ö×Ó£¬Ć»ÓŠ×ŌÓÉŅĘ¶ÆµÄĄė×Ó£¬¶žŃõ»ÆĮņŌŚĖ®ČÜŅŗÖŠÓėĖ®·“Ӧɜ³ÉŃĒĮņĖį£¬ŃĒĮņĖįµēĄė³ö×ŌÓÉŅĘ¶ÆµÄĄė×Óµ¼µē£¬¶žŃõ»ÆĮņ×ŌÉķ²»ÄܵēĄė£¬¶žŃõ»ÆĮņŹĒ·Ēµē½āÖŹ£¬Ń”ĻīB“ķĪó£»
C£®H2SO4ŹĒ¹²¼Ū»ÆŗĻĪļŌŚĖ®ČÜŅŗÖŠÄܹ»µ¼µē£¬ŌŚČŪȌדĢ¬ĻĀ²»µ¼µē£¬¶ųĒŅŹōÓŚµē½āÖŹ£¬Ń”ĻīCÕżČ·£»
D£®BaSO4ŌŚĖ®ČÜŅŗÖŠÄܵ¼µē£¬µ«ŹĒµ¼µēŠŌŗÜČõ£¬ŌŚČŪȌדĢ¬ĻĀ¶¼Äܹ»µ¼µē£¬ŹĒµē½āÖŹ£¬Ń”ĻīD“ķĪó£»
“š°øŃ”C”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¶ĢÖÜĘŚŌŖĖŲX”¢Y”¢ZŌŚÖÜĘŚ±ķÖŠµÄĪ»ÖĆČēĶ¼ĖłŹ¾£¬ŅŃÖŖXÓėYµÄŌ×ÓŠņŹżÖ®ŗĶµČÓŚZµÄŌ×ÓŠņŹż”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ

A. YµÄµ„ÖŹÓėĖ®·“Ó¦Ź±£¬YµÄµ„ÖŹ¼ČŹĒŃõ»Æ¼ĮÓÖŹĒ»¹Ō¼Į
B. XµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļÓėĘäĘųĢ¬Ēā»ÆĪļæÉŅŌ·“Ӧɜ³ÉŃĪ
C. X”¢Y”¢ZŌŖĖŲŠĪ³ÉµÄµ„ÖŹ£¬³£ĪĀĻĀZµ„ÖŹµÄ·Šµć×īµĶ
D. µ„ÖŹµÄŃõ»ÆŠŌ£ŗY£¼Z
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijŠĖȤŠ”×éÉč¼ĘČēĶ¼ĖłŹ¾µÄĪ¢ŠĶŹµŃé×°ÖĆ”£ŹµŃ鏱£¬ĻȶĻæŖK2£¬±ÕŗĻK1£¬Į½¼«¾łÓŠĘųÅŻ²śÉś£»Ņ»¶ĪŹ±¼äŗ󣬶ĻæŖK1£¬±ÕŗĻK2£¬·¢ĻÖµēĮ÷±ķAÖøÕėĘ«×Ŗ”£ĻĀĮŠÓŠ¹ŲĆčŹöÕżČ·µÄŹĒ£Ø £©

A. ¶ĻæŖK2£¬±ÕŗĻK1Ź±£¬×Ü·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗ![]()
B. ¶ĻæŖK2£¬±ÕŗĻK1Ź±£¬ŹÆÄ«µē¼«ø½½üČÜŅŗ±äŗģ
C. ¶ĻæŖK1£¬±ÕŗĻK2Ź±£¬Ķµē¼«ÉĻµÄµē¼«·“Ó¦Ź½ĪŖ£ŗCl2+2e-ØT2Cl-
D. ¶ĻæŖK1£¬±ÕŗĻK2Ź±£¬ŹÆÄ«µē¼«×÷Õż¼«
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¼×”¢ŅŅĮ½Ī»Ń§ÉśĻėĄūÓĆŌµē³Ų·“Ó¦¼ģ²ā½šŹōµÄ»ī¶ÆŠŌĖ³Šņ£¬Į½ČĖ¾łŹ¹ÓĆĆ¾Ę¬ŗĶĀĮʬ×÷µē¼«£¬µ«¼×Ķ¬Ń§½«µē¼«·ÅČė6mol”¤L-1H2SO4ČÜŅŗÖŠ£¬ŅŅĶ¬Ń§½«µē¼«·ÅČė6mol”¤L-1µÄNaOHČÜŅŗÖŠ£¬ČēĻĀĶ¼ĖłŹ¾”£
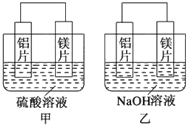
£Ø1£©Čē¹ū¼×”¢ŅŅĶ¬Ń§¾łČĻĪŖČō¹¹³ÉŌµē³ŲµÄµē¼«²ÄĮĻ¶¼ŹĒ½šŹō£¬Ōņ¹¹³Éøŗ¼«²ÄĮĻµÄ½šŹōÓ¦±Č¹¹³ÉÕż¼«²ÄĮĻµÄ½šŹō»īĘĆ£¬Ōņ¼×»įÅŠ¶Ļ³ö______µÄ»ī¶ÆŠŌøüĒ棬¶ųŅŅ»įÅŠ¶Ļ³öøŗ¼«µÄµē¼«·“Ó¦Ź½ĪŖ______________”£
£Ø2£©ÓÉ“ĖŹµŃ飬æɵƵ½ÄÄŠ©ÕżČ·µÄ½įĀŪ£æ___________£ØĢī×ÖÄø£©”£
A.ĄūÓĆŌµē³Ų·“ӦŊ¶Ļ½šŹō»ī¶ÆŠŌĖ³ŠņŹ±Ó¦×¢ŅāŃ”ŌńŗĻŹŹµÄ½éÖŹ
B.Ć¾µÄ½šŹōŠŌ²»Ņ»¶Ø±ČĀĮµÄ½šŹōŠŌĒæ
C.øĆŹµŃéĖµĆ÷½šŹō»ī¶ÆŠŌĖ³Šņ±ķŅŃ¹żŹ±£¬ŅŃƻӊŹµÓĆ¼ŪÖµ
D.øĆŹµŃéĖµĆ÷»Æѧъ¾æµÄ¶ŌĻóø“ŌÓ£¬·“Ó¦ŹÜĢõ¼žÓ°Ļģ½Ļ“ó£¬Ņņ“ĖÓ¦¾ßĢåĪŹĢā¾ßĢå·ÖĪö
£Ø3£©ÉĻŹöŹµŃéŅ²·“¹żĄ“Ö¤Ć÷ĮĖ”°Ö±½ÓĄūÓĆ½šŹō»ī¶ÆŠŌĖ³Šņ±ķÅŠ¶ĻŌµē³ŲµÄÕż”¢øŗ¼«”±µÄ×ö·Ø_________£ØĢī”°æÉææ”±»ņ”°²»æÉææ”±£©”£Čē²»æÉæ棬ĒėÄćĢį³öĮķŅ»øöÅŠ¶ĻŌµē³ŲÕż”¢øŗ¼«µÄæÉŠŠµÄŹµŃé·½°ø£ŗ_______________£¬£ØČēæÉæ棬“ĖæÕæɲ»Ģī£©”£
£Ø4£©ĀĮµē³ŲŠŌÄÜÓÅŌ½£¬Al-Ag2Oµē³ŲæÉÓĆ×÷Ė®ĻĀ¶ÆĮ¦µēŌ“£¬ĘäŌĄķČēĻĀĶ¼ĖłŹ¾”£øƵē³Ų·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ_______________________________”£
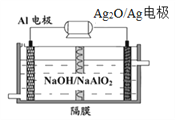
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ¶ŌÉś»īÖŠÓŠ¹Ų»ÆѧĪŹĢāµÄ·ÖĪöÕżČ·µÄŹĒ£Ø””””£©
A.øĘŗĶĮ׶¼ŹĒČĖĢåÄŚŗ¬Įæ·įø»µÄæóĪļŌŖĖŲ£¬ĖüĆĒ¶¼ŹōÓŚĪ¢ĮæŌŖĖŲ
B.Ą¬»ų·ŁÉÕŗĶ·¢µē¼¼ŹõµÄ½įŗĻ£¬¼Č½ā¾öĮĖĪŪČ¾ĪŹĢā£¬ÓÖÓŠŠ§ĄūÓĆĮĖĄ¬»ųĖłŗ¬µÄÄÜĮæ
C.ÖĘŌģĘÕĶز£Į§µÄÖ÷ŅŖ·“Ó¦ŌĄķÖ®Ņ»ĪŖ£ŗCaO+SiO2 ![]() CaSiO3
CaSiO3
D.ĒąĆ¹ĖŲŹĒ×īŌē·¢ĻÖµÄĢģČ»æ¹ÉśĖŲ£¬ĘäÖŠĘšÖĪĮĘ×÷ÓƵďĒĖ®ŃīĖį
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÄÉĆ×Ńõ»ÆīÜŌŚ°ėµ¼ĢåŗĶĪ¢µē×ÓŠŠŅµÓ¦ÓĆ¹ć·ŗ£¬Ä³Š©½šŹō·ĻĮĻÖŠŗ¬ÓŠCoŌŖĖŲ£¬“Ó·ĻĮĻ(ŗ¬Co3O4”¢Al2O3”¢Li2O”¢Fe2O3µČĪļÖŹ) ÖŠÖʱøøß“æ¶ČµÄÄÉĆ×¼¶īܵÄŃõ»ÆĪļ£¬Į÷³ĢČēĻĀ
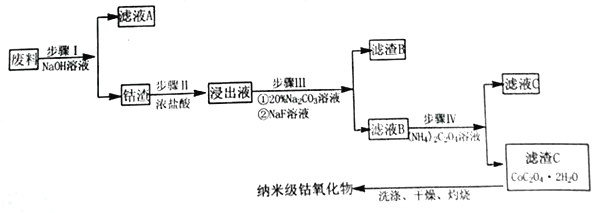
ŅŃÖŖ:
¢ŁLiF ÄŃČÜÓŚĖ®£¬Li2CO3Ī¢ČÜÓŚĖ®£»
¢ŚīÜŌŖĖŲ³£¼ūµÄ»ÆŗĻ¼ŪĪŖ+2 ŗĶ+3£»
¢Ū²æ·Ö½šŹōĄė×ÓŠĪ³ÉĒāŃõ»ÆĪļ³ĮµķµÄpH¼ūĻĀ±ķ”£
Fe3+ | Co2+ | Co3+ | Al3+ | |
pH£ØæŖŹ¼³Įµķ£© | 1.9 | 7.15 | -0.23 | 3.4 |
pH£ØĶźČ«³Įµķ£© | 3.2 | 9.15 | 1.09 | 4.7 |
£Ø1£©²½Öč¢ńÖŠ·¢ÉśµÄĄė×Ó·“Ó¦·½³ĢŹ½_______________£»
£Ø2£©²½ÖčII¼ÓÅØŃĪĖįµÄ×÷ÓĆŹĒ_______________£»
£Ø3£©²½ÖčIIIÖŠNa2CO3ČÜŅŗµÄ×÷ÓĆŹĒµ÷½ŚČÜŅŗµÄpH,Ó¦Ź¹ČÜŅŗµÄpHµÄȔֵ·¶Ī§ĪŖ_______________£» ĀĖŌü B µÄÖ÷ŅŖ³É·ÖĪŖ_________________£»
£Ø4£©¼ņŹöČēŗĪ¼ģŃéĀĖŅŗBÖŠŹĒ·ń»¹ÓŠ²ŠĮōµÄFe3+:_______________£»
£Ø5£© ¾¹ż·“ø“Ļ“µÓ”¢øÉŌļŗó³ĘÖŲ£¬½«ÖŹĮæĪŖ3.66gCoC2O4”¤2H2O½ųŠŠ×ĘÉÕ£¬²ŠĮō¹ĢĢåÖŹĮæČēĶ¼ĖłŹ¾”£
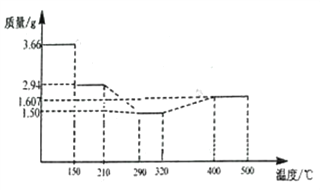
210”ę~290”ꏱČōÉś³ÉĮ½ÖÖĘųĢ壬Ōņ·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ_______________£¬400”ę~500”ęĖłµĆ¹ĢĢåµÄ»ÆѧŹ½ĪŖ_______________£»
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĄąŠĶµÄ·“Ó¦ÖŠ£¬ŌŖĖŲ»ÆŗĻ¼ŪŅ»¶Ø·¢Éś±ä»ÆµÄŹĒ (””””)
A.»ÆŗĻ·“Ó¦B.·Ö½ā·“Ó¦C.ÖĆ»»·“Ó¦D.ø“·Ö½ā·“Ó¦
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĀĮŌŚæÕĘųÖŠÄܹ»ĪČ¶Ø“ęŌŚµÄŌŅņŹĒ
A.ĀĮµÄ»īĘĆŠŌ²īB.ĀĮµÄ»¹ŌŠŌ²ī
C.ĀĮÓėŃõĘų²»·“Ó¦D.ĀĮ±ķĆęÓŠŃõ»ÆĤ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ“ß»ÆĶŁŅŗµķ·ŪĆøĖ®½āµÄĆøŹĒ£Ø £©
A£®ėÄĆø B£®µ°°×Ćø C£®Ö¬·¾Ćø D£®µķ·ŪĆø
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com