
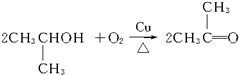 +2H2O����ֻдһ����
+2H2O����ֻдһ�������� ��1�������ܣ����е㲻ͬ��
��2�����������Թ��ڷ�Ӧǰ���������������ΪAg��������
��3��Brԭ����1C�ϳɼ�������CH3CH2CH2Br��ˮ������CH3CH2CH2OH������������CH3CH2CHO���ɷ���������Ӧ��
��4��Brԭ����1C�ϳɼ�������CH3CH2CH2Br��ˮ������CH3CH2CH2OH������������CH3CH2CHO���ɷ���������Ӧ����Ϸ�Ӧ��ԭ���غ�ɼ���Ag����������Brԭ����2C�ϳɼ������ղ��ܵõ�Ag���Դ������
��� �⣺��1�������ܣ����е㲻ͬ�����裨�������ᴿ��ϴ��ļ����������ǣ�������ϴ��Ļ����������ʴ�Ϊ������
��2�������������������ķ���Ϊ��ȡһ֧����ྻ���Թܵ�����m1���ô��Թܽ�������ʵ�飬ʵ����ϣ������Թ��е���Һ��������ˮϴ���Թܼ��Σ�Ȼ���ɣ��ٳ����Թ���ͬ��������m2����m2-m1����Ϊ��������w��
�ʴ�Ϊ����ȡһ֧����ྻ���Թܵ�����m1���ô��Թܽ�������ʵ�飬ʵ����ϣ������Թ��е���Һ��������ˮϴ���Թܼ��Σ�Ȼ���ɣ��ٳ����Թ���ͬ��������m2����m2-m1����Ϊ��������w��
��3�����裨�ģ��е�����һ����ѧ��Ӧ����ʽ2CH3CH2CH2OH+O2$��_{��}^{Cu}$2CH3CH2CHO+2H2O����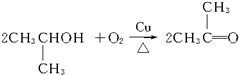 +2H2O����
+2H2O����
�ʴ�Ϊ��2CH3CH2CH2OH+O2$��_{��}^{Cu}$2CH3CH2CHO+2H2O����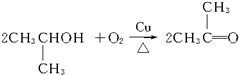 +2H2O����
+2H2O����
��4��Brԭ����1C�ϳɼ�������CH3CH2CH2Br��ˮ������CH3CH2CH2OH������������CH3CH2CHO���ɷ���������Ӧ����CH3CH2CHO+2[Ag��NH3��2]OH$\stackrel{ˮԡ}{��}$CH3CH2COONH4+2Ag��+3NH3+H2O��֪����wΪ$\frac{0.224L}{22.4L/mol}$��2��108g/mol=2.16g��
��Brԭ����2C�ϳɼ������ղ��ܵõ�Ag������wΪ2.16����ϩ����HBr�ļӳɷ�ʽΪ�٣�
��w=0����ϩ����HBr�ļӳɷ�ʽΪ�ڣ�
��0��w��2.16����ϩ����HBr�ӳɵķ�ʽ�٢ھ��У�
�ʴ�Ϊ��2.16��0��0��w��2.16��
���� ���⿼�����ʵ���ɼ��л���Ľṹ�����ʣ�Ϊ��Ƶ���㣬������ѧ���ķ�����ʵ�������Ŀ��飬�����л���Ĺ����ŵ�����Ϊ������Ĺؼ�����Ŀ�ѶȲ���ע�Ⲯ������������ȩ��ȩ����������Ӧ��


 ��˼ά������ҵ��ټ��ִ�ѧ������ϵ�д�
��˼ά������ҵ��ټ��ִ�ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
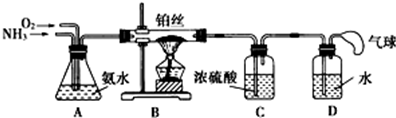
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ȼ�ϵ����һ�ָ�Ч�������Ѻõ����͵�� | |
| B�� | Ǧ���طŵ��ʱ��������Pb��������PbO2 | |
| C�� | �����ء�����ӵ�غͼ���п�̸ɵ�ض��Ƕ��ε�� | |
| D�� | ԭ������������ķ�Ӧ��������Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 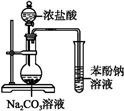 ֤�����ԣ����̼����� | B�� |  ʵ������ȡ�������� | ||
| C�� |  ʯ�ͷ��� | D�� |  ʵ������ȡ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | C7H8O | B�� | C3H8 | C�� | C2H4Br2 | D�� | C3H6O2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
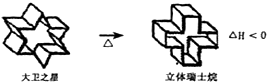
| A�� | ����������ķ���ʽΪC24H26 | |
| B�� | ����֮������������ʿ���һ�ȴ����ֻ��һ�� | |
| C�� | ����֮�����������ʿ����ȶ� | |
| D�� | ����֮������������ʿ�黥Ϊͬ���칹�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������Һ��ͨ��CO2���壺SiO32-+H2O+CO2�TH2SiO3��+CO32- | |
| B�� | �������백ˮ��Ӧ��Al3++3NH3•H2O�TAl��OH��3��+3NH4+ | |
| C�� | ����������������Һ��Ӧ��Cl2+OH-�TCl-+ClO-+H2O | |
| D�� | С�մ���Һ��ϡ���ᷴӦ��CO32-+2H+�TH2O+CO2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �� ���� | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | �� | �� | ||||||
| 3 | �� | �� | �� | �� | �� | |||
| 4 | �� | �� | �� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com