
水热法制备纳米颗粒Y(化合物)的反应为3Fe2++2S2O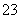 +O2+aOH-===Y+S4O
+O2+aOH-===Y+S4O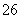 +2H2O,下列说法中,不正确的是( )
+2H2O,下列说法中,不正确的是( )
A.a=4
B.Y的化学式为Fe2O3
C.S2O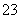 是还原剂
是还原剂
D.每有1 mol O2参加反应,转移的电子为4 mol
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
根据物质中N元素的化合价判断,下列说法错误的是( )
A.NH3具有还原性
B.N2既具有氧化性又具有还原性
C.N2只具有氧化性
D.HNO3具有氧化性
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)25 ℃、101 kPa时,1 g甲醇完全燃烧生成CO2和液态水,放出22.68 kJ热量,则该反应的热化学方程式为________________________________________。
(2)0.3 mol气态高能燃料乙硼烷(B2H6)在O2中燃烧,生成固态B2O3和液态水,放出649.5 kJ热量,则该反应的热化学方程式为______________
______________________________________________________________。
(3)肼(N2H4)是一种高效清洁的火箭燃料。0.25 mol N2H4(g)完全燃烧生成氮气和气态水时,放出133.5 kJ热量,则肼燃烧的热化学方程式为______________________________________________________________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
前四周期原子序数依次增大的元素A、B、C、D中,A和B的价电子层中未成对电子均只有1个,并且A-和B+的电子数相差为8;与B位于同一周期的C和D,它们价电子层中的未成对电子数分别为4和2,且原子序数相差为2。
回答下列问题:
(1)D2+的价层电子排布图为________。
(2)四种元素中第一电离能最小的是________,电负性 最大的是________。(填元素符号)
最大的是________。(填元素符号)
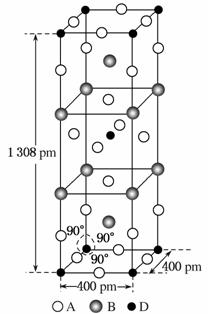
(3)A、B和D三种元素组成的一个化合物的晶胞如图所示。
①该化合物的化学式为________;D的配位数为________;
②列式计算该晶体的密度________g·cm-3。
(4)A-、B+和C3+三种离子组成的化合物B3CA6,其中化学键的类型有________;该化合物中存在一个复杂离子,该离子的化学式为________,配位体是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂等的漂白与杀菌。下图是用过氧化氢法生产亚氯酸钠晶体的工艺流程图:
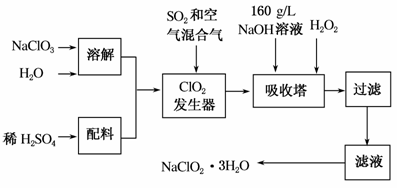
已知:①NaClO2的溶解度随温度升高而增大。
②纯ClO2气体易分解爆炸。
(1)发生器中鼓入空气的作用可能是________(填选项字母,下同)。
a.将SO2氧化成SO3,增强酸性
b.稀释ClO2以防止爆炸
c.将NaClO3氧化成ClO2
(2)吸收塔内发生反应的化学方程式为________________________ _________________。吸收塔内的温度不能超过20 ℃,原因是_____________________________________________________________。
(3)在碱性溶液中NaClO2比较稳定,所以吸收塔中应维持NaOH稍过量,判断NaOH是否过量的简单实验方法是__________________________。
(4)吸收塔中为防止NaClO2被还原成NaCl,所用还原剂的还原性应适中。除H2O2外,还可以选择的还原剂是________。
a.Na2O2 b.Na2S c.FeCl2
(5)从滤液中得到NaClO2·3H2O粗晶体的实验操作依次是________。
a.蒸馏 b.蒸发浓缩 c.灼烧 d.过滤
e.冷却结晶
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子组在水溶液中能大量共存,且投入铝有气体生成的是( )
A.NO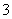 、Cl-、Na+、H+
、Cl-、Na+、H+
B.AlO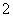 、K+、ClO-、CO
、K+、ClO-、CO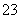
C.Ca2+、Cl-、SO 、Na+
、Na+
D.SO 、Fe2+、OH-、NH
、Fe2+、OH-、NH
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.乙酸的酸性比碳酸强,所以它可以跟碳酸盐溶液反应,产生CO2气体
B.乙酸酸性较弱,不能使紫色石蕊试液变红
C.乙酸分子中含有碳氧双键,所以它能与溴发生加成反应使溴水褪色
D.酯化反应不属于取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:①A从石油中获得是目前工业上生产的主要途径,A的产量通常用来衡量一个国家的石油化工发展水平;②2CH3CHO+O2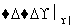 2CH3COOH。现以A为主要原料合成乙酸乙酯,其合成路线如下图所示。
2CH3COOH。现以A为主要原料合成乙酸乙酯,其合成路线如下图所示。

回答下列问题:
(1)写出A的结构简式________________________________________________________________________。
(2)B、D分子中的官能团名称分别是________、________。
(3)写出下列反应的反应类型:
①________,②________,④________。
(4)写出下列反应的化学方程式:
①________________________________________________________________________;
②________________________________________________________________________;
④________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
绿矾(FeSO4·7H2O)是治疗缺铁性贫血药品的重要成分。下面是以市售铁屑(含少量锡、氧化铁等杂质)为原料生产纯净绿矾的一种方法:
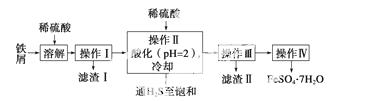
查询资料,得有关物质的数据如下表:
| 25 ℃时 | pH |
| 饱和H2S溶液 | 3.9 |
| SnS沉淀完全 | 1.6 |
| FeS开始沉淀 | 3.0 |
| FeS沉淀完全 | 5.5 |
(1)检验制得的绿矾晶体中是否含有Fe3+,最好选用的试剂为________(填字母序号)。
A.KSCN溶液 B.NaOH溶液
C.KMnO4溶液 D.苯酚溶液
(2)操作Ⅱ中,通入硫化氢至饱和的目的是______________________;在溶液中用硫酸酸化至pH=2的目的是____________________。
(3)操作Ⅳ的顺序依次为____________、冷却结晶、___________________________。
(4)操作Ⅳ得到的绿矾晶体用少量冰水洗涤,其目的是①除去晶体表面附着的硫酸等杂质;②__________________________________________________________________。
(5)测定绿矾产品中Fe2+含量的方法:a.称取2.850 g绿矾产品,溶解,在250 mL容量瓶中定容;b.量取25.00 mL待测溶液于锥形瓶中;c.用硫酸酸化的0.010 00 mol·L-1 KMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00 mL。
①滴定时盛放KMnO4溶液的仪器为________________(填仪器名称)。
②判断此滴定实验达到终点的方法是________________________________________。
③上述样品中FeSO4·7H2O的质量分数为________。(结果保留3位有效数字)(FeSO4·7H2O的相对分子质量为278)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com