
【题目】下列原子半径最大的是( )
A.OB.FC.NaD.S
 同步轻松练习系列答案
同步轻松练习系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是(NA表示阿伏加德罗常数的值)( )
A. 物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl- 个数为NA
B. 标准状况下,18 g H2O所占的体积约是22.4 L
C. 32 g O2在标准状况下所占的体积约为22.4 L
D. 2.4g金属镁变为镁离子时失去的电子数为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】只用下列一种试剂,就能将Ba(NO3)2、NaAlO2、NaHCO3、AlCl3四种无色透明溶液区别开来,这种试剂是 ( )
A. 硫酸 B. 盐酸 C. 氨水 D. 氢氧化钠溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电化学在日常生活中用途广泛,图甲是镁—次氯酸钠燃料电池,电池总反应为:Mg+ClO-+H2O=Cl-+Mg(OH)2↓,图乙是含Cr2O72-的工业废水的处理。下列说法正确的是( )
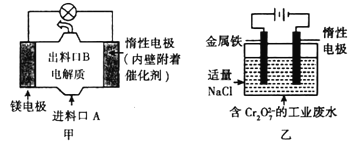
A. 图甲中发生的还原反应是Mg2++ClO-+H2O+2e-=Cl-+Mg(OH)2↓
B. 图乙中Cr2O72-向惰性电极移动,与该极附近的OH-结合,转化成Cr(OH)3除去
C. 图乙电解池中,若有0.84 g阳极材料参与反应,则阴极会有168 mL(标准状况)的气体产生
D. 若图甲燃料电池消耗0.36 g镁产生的电量用以图乙废水处理,理论上可产生1.07g氢氧化铁沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列做法与环保理念不符合的是
A. 采用增大臭氧浓度来改善空气质量 B. 利用地热、潮汐等能源替代化石燃料
C. 使用可降解塑料减少“白色污染” D. 选用不含氮、磷的洗涤剂防止蓝藻污染
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需配制0.5 mol·L-1的烧碱溶液500mL,根据配制的过程,完成填空:
(1)根据计算得知,所需NaOH固体用托盘天平称出的质量为___________g。
(2)配制溶液的过程中,有以下操作。其中正确的是___________ (填序号)。
A.将氢氧化钠固体放在纸片上称量
B.在烧杯中溶解氢氧化钠固体后,立即将溶液倒入容量瓶中
C.将溶解氢氧化钠的烧杯用蒸馏水洗涤2~3次,并将洗涤液转移到容量瓶中
D.定容时发现所配溶液超过刻度线,用胶头滴管吸取溶液使液面与刻度线相平
(3)玻璃棒在该实验中的作用有:
①_______________。
②_______________。
(4)若出现如下情况,对所配溶液浓度将有何影响(填“偏高”、“偏低”或“无影响”)?
①若没有将洗涤液转移到容量瓶的操作_______________;
②若加蒸馏水时不慎超过了容量瓶的刻度_______________;
③若定容时俯视刻度线_______。
④容量瓶中使用前有少量蒸馏水没有干燥_______。
(5)取所配溶液24.0 mL可以中和_______mL的12mol/L浓盐酸。标准状况下_______L的HCl气体溶于水可配成这种浓度的浓盐酸100 mL。
(6)计算填空:已知MnO2+4HCl (浓)![]() MnCl2+Cl2↑+2H2O。若用二氧化锰消耗此12mol/L 的浓盐酸100 mL制备氯气,理论上需要二氧化锰_______g,可以制得氯气在标准状况下的体积为_______L。该反应是否是氧化还原反应,请判断并说出理由_______。
MnCl2+Cl2↑+2H2O。若用二氧化锰消耗此12mol/L 的浓盐酸100 mL制备氯气,理论上需要二氧化锰_______g,可以制得氯气在标准状况下的体积为_______L。该反应是否是氧化还原反应,请判断并说出理由_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在容积固定的V L密闭容器中加入n mol A、2n mol B,发生反应:
A(g)+2B(g) ![]() 2C(g) ΔH<0,反应达平衡后测得平衡常数为K,此时A的转化率为x。
2C(g) ΔH<0,反应达平衡后测得平衡常数为K,此时A的转化率为x。
(1)一段时间后上述反应达到平衡。则下列说法中正确的是________(填字母)。
A.物质A、B的转化率之比为1∶2
B.起始时刻和达到平衡后容器中的压强之比为3n∶(3n-nx)
C.当2v正(A)=v逆(B)时,反应一定达到平衡状态
D.充入惰性气体(如Ar),平衡向正反应方向移动
(2)K和x的关系满足K=______________。在保证A浓度不变的情况下,扩大容器的体积,平衡________(填字母)。
A.向正反应方向移动
B.向逆反应方向移动
C.不移动
(3)该反应的逆反应速率与时间的关系如图所示。

①由图可知,反应在t1、t3、t7时都达到了平衡,而t2、t8时都改变了一种条件,试判断改变的条件:
t2时____________________________________________________________________;
t8时____________________________________________________________________。
②t2时平衡向________(填“正反应”或“逆反应”)方向移动。
③若t4时降压,t5时达到平衡,t6时增大反应物的浓度,请在图中画出t4~t6时逆反应速率与时间的关系线。______
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com