
| A£® | “óĮ¦·ĄÖĪ PM2.5 µÄĪŪČ¾·ĄÖĪ£¬æɼõÉŁĪķö²ĢģĘų | |
| B£® | ”°84 Ļū¶¾Ņŗ”±¾ßÓŠĒæŃõ»ÆŠŌ£¬æÉ×÷»·¾³µÄĻū¶¾¼Į | |
| C£® | ·¢Õ¹µĶĢ¼¾¼Ć£¬ĄūÓĆĢ«ŃōÄÜ”¢·ēÄÜŹµĻÖ³ĒŹŠÕÕĆ÷ | |
| D£® | æÉŅŌÓĆø£¶ūĀķĮÖČÜŅŗ±£“ęŗ£ĻŹ²śĘ· |
·ÖĪö A£®PM2.5ŹĒŠĪ³ÉĪķö²ĢģĘųµÄÖ÷ŅŖŌŅņÖ®Ņ»£®
B£®84”±Ļū¶¾Ņŗ£¬ĘäÖ÷ŅŖ³É·ÖŹĒNaClO£¬NaClOÄÜÓėĖ®”¢¶žŃõ»ÆĢ¼Éś³É“ĪĀČĖį£¬“ĪĀČĖį¾ßÓŠĒæŃõ»Æ¼Į£»
C£®Ģ«ŃōÄÜ”¢·ēÄÜŹĒĒå½ąÄÜŌ“£»
D£®ø£¶ūĀķĮÖÓŠ¶¾£¬²»Äܱ£“ęŗ£ĻŹ£®
½ā“š ½ā£ŗA£®PM2.5ŹĒŠĪ³ÉĪķö²ĢģĘųµÄÖ÷ŅŖŌŅņÖ®Ņ»£¬PM2.5ŹōÓŚæÕĘųĪŪČ¾Īļ£¬æŲÖĘPM2.5µÄÅÅ·ÅæÉŅŌ¼õÉŁĪķö²ĢģĘų£¬ÓŠĄūÓŚĢįøßæÕĘųÖŹĮ棬¹ŹAÕżČ·£»
B£®84”±Ļū¶¾Ņŗ£¬ĘäÖ÷ŅŖ³É·ÖŹĒNaClO£¬NaClOÄÜÓėĖ®”¢¶žŃõ»ÆĢ¼Éś³É“ĪĀČĖį£¬“ĪĀČĖį¾ßÓŠĒæŃõ»ÆŠŌ£¬æÉÓÉӌɱ¾śĻū¶¾£¬¹ŹBÕżČ·£»
C£®Ģ«ŃōÄÜ”¢·ēÄÜŹĒĒå½ąÄÜŌ“£¬ĄūÓĆĢ«ŃōÄÜ”¢·ēÄÜŹµĻÖ³ĒŹŠÕÕĆ÷£¬æɼõÉŁ¶žŃõ»ÆĢ¼µÄÅÅ·Å£¬¹ŹCÕżČ·£»
D£®ø£¶ūĀķĮÖĪŖ¼×Č©µÄĖ®ČÜŅŗ£¬¼×Č©ÓŠ¶¾£¬Ōņ²»ÄÜÓĆø£¶ūĀķĮÖČÜŅŗ±£“ęŗ£ĻŹ²śĘ·£¬¹ŹD“ķĪó£»
¹ŹŃ”D£®
µćĘĄ ±¾Ģāæ¼²é½ĻĪŖ×ŪŗĻ£¬Éę¼°»·¾³ĪŪČ¾¼°ÖĪĄķ”¢¼×Č©”¢“ĪĀČĖįÄʵĊŌÖŹ¼°Ó¦ÓƵČÖŖŹ¶£¬ĢāÄæÄѶČÖŠµČ£¬Ć÷Č·³£¼ūĪļÖŹ×é³É”¢½į¹¹ÓėŠŌÖŹĪŖ½ā“š¹Ų¼ü£¬ŹŌĢāÅąŃųĮĖѧɜµÄ·ÖĪöÄÜĮ¦¼°Įé»īÓ¦ÓĆ»ł“”ÖŖŹ¶µÄÄÜĮ¦£¬ÓŠĄūÓŚĢįøßѧɜµÄ»·±£ŅāŹ¶£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | ÓĆ¹ęøńĪŖ100mLµÄĮæĶ²ĮæČ”89.7mLÕōĮóĖ® | |
| B£® | ÓĆČŻĮæĘæÅäÖĘŅ»¶ØĪļÖŹµÄĮæÅØ¶ČµÄČÜŅŗĒ°ŠčÓƱź×¼ŅŗČóĻ“ | |
| C£® | “ņæŖ·ÖŅŗĀ©¶·”¢³¤¾±Ā©¶·”¢µĪŅŗĀ©¶·µÄ»īČū£¬¾łæɷųöĘäÖŠŅŗĢå | |
| D£® | ׶ŠĪĘ攢ÉÕ±”¢ÉÕĘæ¾łæɵę¼ÓŹÆĆŽĶų¼ÓČČ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | HNO3ČÜŅŗ£ØH2SO4£©£¬ŹŹĮæBaCl2ČÜŅŗ£¬¹żĀĖ | |
| B£® | Fe2+£ØFe3+£©£¬»¹ŌĢś·Ū£¬¹żĀĖ | |
| C£® | Cl2£ØHCl£©£¬±„ŗĶŹ³ŃĪĖ®£¬Ļ“Ęų | |
| D£® | CO2£ØSO2£©£¬±„ŗĶNaHCO3ČÜŅŗ”¢ÅØĮņĖį£¬Ļ“Ęų |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
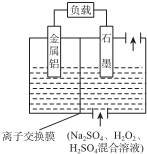
| A£® | ĀĮ×÷øƵēŌ“µÄøŗ¼«£¬µē¼«·“Ó¦ĪŖ£ŗAl-3e-ØTAl3+ | |
| B£® | µē³Ų×Ü·“Ó¦£ŗ2Al+3H2O2+6H+ØT2Al3++6H2O | |
| C£® | ·ÅµēŹ±ČÜŅŗÖŠµÄSO42-ĻņÕż¼«ŅĘ¶Æ | |
| D£® | ·ÅµēŹ±Õż¼«ÖÜĪ§ČÜŅŗµÄpHÉżøß |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | øƵē³Ų·ÅµēŹ±£¬ĶØČėėĀµÄŅ»¼«ĪŖøŗ¼« | |
| B£® | µē³ŲĆæŹĶ·Å1molN2×ŖŅʵĵē×ÓŹżĪŖ4NA | |
| C£® | µē³Ų¹¤×÷Ņ»¶ĪŹ±¼äŗ󣬵ē½āÖŹČÜŅŗµÄpH½«²»±ä | |
| D£® | ĶØČėæÕĘųµÄŅ»¼«µÄµē¼«·“Ó¦Ź½ŹĒ£ŗO2+2H2O+4e-=4OH- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
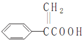 £®ĻĀĮŠÓŠ¹ŲĖµ·ØÖŠ“ķĪóµÄŹĒ£Ø””””£©
£®ĻĀĮŠÓŠ¹ŲĖµ·ØÖŠ“ķĪóµÄŹĒ£Ø””””£©| A£® | äåµ„ÖŹÄÜÓė°¢ĶŠĖį·¢Éś¼Ó³É·“Ó¦ | |
| B£® | °¢ĶŠĖįÄÜÓėĻõĖį·¢ÉśČ”“ś·“Ó¦ | |
| C£® | æÉÓĆĖįŠŌKMnO4ČÜŅŗĒų±š°¢ĶŠĖįÓė±½ | |
| D£® | °¢ĶŠĖį·Ö×ÓÖŠŗ¬ÓŠ4øöĢ¼Ė«¼ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 3ÖÖ | B£® | 8ÖÖ | C£® | 16ÖÖ | D£® | 24ÖÖ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com