
元素在周围表中的位置,反映了元素的原子结构和元素的性质,下列说法正确的是( )
A.同一元素不可能既表现金属性,又表现非金属性
B.第三周期主族元素的最高正化合价等于它所处的主族序数
C.短周期元素形成离子后,最外层都达到8电子稳定结构
D.同一主族的元素的原子,最外层电子数相同,化学性质完全相同
科目:高中化学 来源:2016届浙江省湖州市属九校高一12月联考化学试卷(解析版) 题型:填空题
下图表示在没有通风橱的条件下制备氯气时设计的装置,图中a、b是可控制的弹簧铁夹。(氯气在饱和氯化钠溶液中的溶解度较小。)
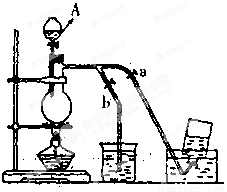
(1)仪器A的名称是 ;水槽中应盛放的是 ;烧杯中盛放的是 ;烧瓶中反应的化学方程式 ;
在收集氯气时,应打开 关闭 (填a, b)当氯气收集完毕,尾气处理时烧杯中发生反应的离子方程式 。
查看答案和解析>>
科目:高中化学 来源:2016届浙江省杭州市高一上学期期末模拟考试化学试卷(解析版) 题型:选择题
2011年3月11日,在日本发生的9.0级特大地震和随之而来的海啸,造成了福岛核电站的核泄漏事故,在核电站周围检测到的放射性物质包括碘—131、铯—137和钚—239等。其中,碘—131一旦被人体吸入,可能会引发甲状腺疾病,铯—137则会造成人体造血系统和神经系统损伤,钚—239的半衰期达到2.41万年,对人体的危害更大。硼酸具有阻止反应堆内核分裂,降低反应堆温度的功能。下列说法正确的是( )
A. 钚—239的质子数为239 B.氢氧化铯的碱性比氢氧化钾强
C.碘元素的相对原子质量为131 D.硼酸的酸性比铝酸(氢氧化铝)弱
查看答案和解析>>
科目:高中化学 来源:2016届浙江省高一下学期期中考试化学试卷(解析版) 题型:选择题
下列各组物质中,按熔点由低到高排列正确的是( )
A.O2、I2、Hg B.CO2、KCl、SiO2
C.HF、HCl、HI D.SiO2、NaCl、SO2
查看答案和解析>>
科目:高中化学 来源:2016届浙江省高一下学期期中考试化学试卷(解析版) 题型:选择题
纳米是长度单位,1纳米等于1×10-9米,物质的颗粒达到纳米级时,具有特殊的性质。例如
将单质铜制成“纳米铜”时,具有非常强的化学活性,在空气中可以燃烧。下列对“纳米铜” 的有关叙述正确的是( )
A.常温下“纳米铜”比铜片的还原性强,反应时反应速率快
B.“纳米铜”颗粒更细小,化学反应时接触面大,所以反应速率快
C.“纳米铜”与铜是同素异形体
D.常温下“纳米铜”比铜片更易得电子,反应时反应速率快
查看答案和解析>>
科目:高中化学 来源:2016届浙江省宁波市高一上学期期末考试化学试卷(解析版) 题型:填空题
(1)某化学兴趣小组为了探究Cl2的相关性质,设计了如下的实验。
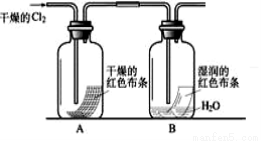
①写出Cl2与水反应的离子方程式 。
②通入Cl2后,从集气瓶A、B的现象可得出的结论是 ;从化学实验的安全环保角度考虑,你认为还应增加的装置是 。
(2)①如图所示,上述实验过程中,不会产生气体的是 ;
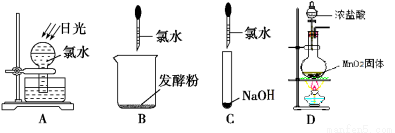
②写出反应D的化学方程式 。
(3)碘是人体中不可缺少的微量元素,食盐中加入碘元素能有效防止缺碘引起的疾病。以前在食盐中加入碘化钾(KI),放置一年后,碘流失约92%。现在食盐中加入碘酸钾(KIO3),在相同条件下碘仅损失约7%。
①食盐中加入碘化钾的碘损失率高的原因是 ;
②萃取碘水中的碘时,一般选用的试剂是(填字母) ;
A.酒精 B.四氯化碳 C.醋酸 D.硝酸银溶液
③可用盐酸酸化的碘化钾和淀粉溶液检验食盐中的碘酸钾。反应的化学方程式为:
5KI+KIO3 + 6HCl = 6KCl + 3I2 + 3H2O,反应的现象是 。
查看答案和解析>>
科目:高中化学 来源:2016届浙江省宁波市高一上学期期末考试化学试卷(解析版) 题型:选择题
下列各组离子能在酸性溶液里大量共存,且溶液呈无色透明的是
A.MnO4-、K+、Na+、SO42-
B.NH4+、Fe2+、SO42-、Cl-
C.Mg2+、SO42-、Cl-、Na+
D.Na+、K+、HCO3-、SO42-
查看答案和解析>>
科目:高中化学 来源:2016届浙江省宁波市八校高一上学期期末联考化学试卷(解析版) 题型:填空题
(14分) 某化学小组模拟“侯氏制碱法”,以NaCl、NH3、CO2和水等为原料以及下图所示装
某化学小组模拟“侯氏制碱法”,以NaCl、NH3、CO2和水等为原料以及下图所示装
置制取NaHCO3,反应的化学方程式为NH3+CO2+H2O+NaCl = NaHCO3↓+NH4Cl。然后再将NaHCO3制成
Na2CO3。

(1)装置乙的作用是 。为防止污染空气,尾气中含有的 需要进行吸收处理。
(2)由装置丙中产生的NaHCO3制取Na2CO3时,需要进行的实验操作有 、 、 。
NaHCO3转化为Na2CO3的化学方程式为 。
(3)若在(2)中灼烧的时间较短,NaHCO3将分解不完全,该小组对一份加热了t1 min的NaHCO3 样品的组成进行了以下探究。
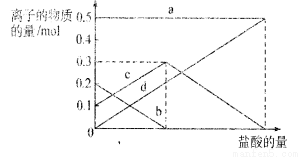
取加热了t1 min的NaHCO3样品29.6 g完全溶于水制成溶液,然后向此溶液中缓慢地滴加稀盐酸,并不断搅拌。随着盐酸的加入,溶液中有关离子的物质的量的变化如右图所示。
则曲线c对应的溶液中的离子是
(填离子符号);该样品中NaHCO3和Na2CO3的物质的量之比是 。
(4)若取21. 0 g NaHCO3固体,加热了t2 min后,剩余固体的质量为l4.8 g。如果把此剩余固体全部加入到200 mL 2 mol·L-1的盐酸中则充分反应后溶液中H+ 的物质的量浓度为____________(设溶液体积变化忽略不计)。
查看答案和解析>>
科目:高中化学 来源:2016届浙江省高一下学期第一次质量检测化学试卷(解析版) 题型:选择题
有一无色混合物水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Fe3+、CO32-、SO42-、H+,现取三份100mL溶液进行如下实验:
⑴ 第一份加入足量AgNO3溶液有沉淀产生
⑵ 第二份加足量NaOH溶液加热后,收集到气体0.04mol
⑶ 第三份加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g。 根据上述实验,以下推测正确的是
A.K+一定存在 B.100mL溶液中含0.01mol CO32-
C.Cl-一定存在 D.Fe3+一定不存在,Mg2+可能存在
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com