
| A��������ȼ����Ϊ241.8 kJ/mol |
| B��1 mol H2O(l)�����������1 mol H2O(g)������� |
| C����Ӧ���Ȼ�ѧ����ʽΪ��2H2(g)��O2(g)===2H2O(g)����H����483.6 kJ/mol |
| D��2 mol H2(g)��1 mol O2(g)���е������ܺʹ���2 mol H2O(g)���е����� |


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����CH3COOH��Һ�м�ˮ��c(OH��)��c(H+)������ |
| B�����ʵ���Ũ�Ⱦ�Ϊ0.1mol?L��1��CH3COOH��Һ��NaOH��Һ�������ϣ�c(Na+)>c(CH3COO��) |
| C��ijŨ�ȵ��Ȼ����Һ�д���c(NH4+)>c(Cl��)>c(H+)> c(OH��) |
| D����pH=4���Ȼ����Һ��c(H+)+ c(NH4+)=" c(Cl��)+" c(OH��) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
A��c(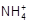 )��c(Cl��)��c(H+)��c(OH��) )��c(Cl��)��c(H+)��c(OH��) | B��c(Cl��)��c(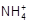 )��c(OH��)��c(H+) )��c(OH��)��c(H+) |
C��c(Cl��)��c(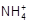 )��c(H+)��c(OH��) )��c(H+)��c(OH��) | D��c(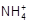 )��c(H+)��c(Cl��)��c(OH��) )��c(H+)��c(Cl��)��c(OH��) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��pH=2��pH=1��������c��H+��֮��Ϊ1:10 |
| B��0.2 mol/L��0.1 mol/L������c��H+��֮��Ϊ2:1 |
| C������ʱ��0.1mol/L ijһԪ��HA��ˮ����0.1%�������룬�����Һ��pH��4 |
| D��25 ��ʱ��pH��13��1.0 L Ba(OH)2��Һ�к��е�OH�� ��ĿΪ0.2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����pH=11������������Һ��ˮϡ��100������Һ��c(H+)=10-13mol/L |
| B����pH=9������������Һ��pH=13������������Һ�������ϣ����û����Һ��pH=11 |
| C����pH=1��������Һ��pH=5������������ϣ����û����Һ��pH=1.3 |
| D��pH=13������������Һ��pH=1������������ϣ�������������������������Һ��pH>7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��ʯ���ѻ��õ���̬ϩ�� | B��ʯ���ѽ�Ŀ������ת�������� |
| C���ҹ����������䡱���̵���ָ���� | D��ˮú����ͨ��ú��Һ���õ�������ȼ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��ȼ��ȼ��ʱ����ѧ��ȫ��ת��Ϊ���� |
| B����ɫֲ����й������ʱ����̫����ת��Ϊ��ѧ�ܡ����桱���� |
| C�����ʵĻ�ѧ�ܿ����ڲ�ͬ������תΪ���ܡ�����Ϊ���������� |
| D����ʯȼ���̲ص���������Զ��ʱ�����������������õ�̫���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����ȼ���Ƿ��Ӿ��壬�۷е�� |
| B��CH4���ӽṹ�ǶԳƵ� |
| C��H2O�ǷǼ��Է��� |
| D��ʹ�ÿ�ȼ�����ú��ʯ�ͣ����Խ���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�������ʵ���Ũ�ȵ�������Һ�У���NH4Al(SO4)2����NH4Cl����CH3COONH4��NH3��H2O��c(NH4+)�ɴ�С��˳���Ǣ�>��>��>�� |
| B�������£���0.01 mol��L��1 NH4HSO4��Һ�еμ�NaOH��Һ�����ԣ�c(Na��)>c(SO42��)>c(NH4+)>c(OH��)��c(H��) |
| C����0.2 mol��L��1 NaHCO3��Һ�м�������0.1 mol��L��1 NaOH��Һ��c(CO32��)>c(HCO3��)>c(OH��)>c(H��) |
| D�����ʵ���Ũ�Ⱦ�Ϊ1 mol��L��1��NaCl��MgCl2���Һ1 L�У�����Cl-����ĿΪ3NA(NA��ʾ�����ӵ�������ֵ��) |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com