
乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物。下列说法正确的是
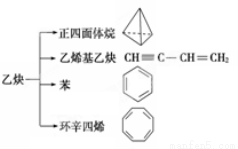
A.正四面体烷的分子式为C4H4,其二氯代物有两种
B.等质量的乙炔与乙烯基乙炔完全燃烧时的耗氧量相同
C.苯为平面六边形结构,分子中存在C—C和C==C,能使酸性KMnO4溶液褪色
D.环辛四烯跟苯的结构很像,不能使溴水褪色
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案科目:高中化学 来源:2013-2014浙江省宁波市高一下学期期末考试化学试卷(解析版) 题型:选择题
下列关于教材中的各项说法错误的一项是( )
A.在化学反应中,反应物转化为生成物的同时,必然发生能量的变化
B.氮肥包括铵态氮肥、硝态氮肥和尿素
C.在书写热化学方程式时应标明反应物及生成物的状态,无需标明反应温度和压强
D.医疗上用的石膏绷带是利用熟石膏与水混合成糊状后很快凝固的性质
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省下学期第二次统练高二化学试卷(解析版) 题型:选择题
下列说法正确的是
A.第一电离能越小的元素其单质金属活泼性一定越大
B.电负性越小的元素金属性一定越强
C.元素电负性相差小于1.7的元素之间形成的化学键一定为共价键
D.制造光电材料的元素主要从IA族中寻找其主要原因是IA的第一电离能比较低
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省下学期第二次统练高一化学试卷(解析版) 题型:选择题
有机物的化学性质主要由其官能团决定。苹果酸是一种有机酸,结构简式为:
 。下列有关苹果酸的说法不正确的是
。下列有关苹果酸的说法不正确的是
A.1mol苹果酸足量金属钠反应,生成氢气3g
B.1mol苹果酸与足量氢氧化钠溶液反应,消耗3 mol氢氧化钠
C.1mol苹果酸能与足量的碳酸氢钠溶液反应,标况下生成44.8L的二氧化碳气体
D.苹果酸在一定条件下既能与醋酸反应,又能与乙醇反应,也可以自身发生酯化反应
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省下学期第二次统练高一化学试卷(解析版) 题型:选择题
下列除杂所用的试剂与方法都正确的是
A.除去NO中混有的NO2:水、洗气
B.除去乙酸乙酯中混有的少量乙酸:氢氧化钠溶液、分液
C.除去乙醇中的少量水:金属钠、蒸馏
D.除去二氧化硫中混有的少量二氧化碳:澄清石灰水、洗气
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省下学期第二次统练高一化学试卷(解析版) 题型:选择题
下列各组物质,化学键类型相同、晶体类型也相同的是
A.SO2和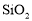 B. CCl4和KCl C.NaCl和HCl D.CO2和H2S
B. CCl4和KCl C.NaCl和HCl D.CO2和H2S
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江省五校高三第二次联考理综化学试卷(解析版) 题型:填空题
(15分)已知2A(g)+B(g) 2C(g),?H=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2 mol A和1 mol B,在500 ℃时充分反应达平衡后C的浓度为ω mol/L,放出热量为b kJ。
2C(g),?H=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2 mol A和1 mol B,在500 ℃时充分反应达平衡后C的浓度为ω mol/L,放出热量为b kJ。
⑴比较a b(填“>”“=”或“<”)。
⑵下表为不同温度下该反应的平衡常数。由此可推知,表中T1 T2(填“>”、“=”或“<”)。
T/K | T1 | T2 | T3 |
K | 1.00×107 | 2.45×105 | 1.88×103 |
若在原来的容器中,只加入2 mol C,500 ℃时充分反应达平衡后,吸收热量为c kJ,C的浓度 (填“>”“=”或“<”)ωmol/L,a、b、c之间满足何种关系 (用代数式表示)。
⑶ 在相同条件下要想得到2a kJ热量,加入各物质的物质的量可能是 。
A. 4 mol A和2 mol BB. 4 mol A、2 mol B和2 mol C
C. 4 mol A和4 mol BD. 6 mol A和4 mol B
⑷为使该反应的反应速率增大,且平衡向正反应方向移动的是 。
A. 及时分离出C气体B. 适当升高温度
C. 增大B的浓度D. 选择高效催化剂
⑸ 若将上述容器改为恒压容器(反应前体积相同),起始时加入2 mol A和1 mol B,500 ℃时充分反应达平衡后,放出热量为d kJ,则d b(填“>”、“=”或“<”),理由是_ 。
⑹ 在一定温度下,向一个容积可变的容器中,通入3 mol A和2 mol B及固体催化剂,使之反应,平衡时容器内气体物质的量为起始时的90%。保持同一反应温度,在相同容器中,将起始物质的量改为4 mol A、3 mol B和2 mol C,则平衡时A的百分含量 (填“不变”、“变大”、“变小”或“无法确定”)。
查看答案和解析>>
科目:高中化学 来源:2013-2014浙江宁波市下学期期末全市(八校)联考高一化学试卷(解析版) 题型:选择题
取100mL Fe(NO3)3与Cu(NO3)2的混合液,若这两种溶液物质的量浓度相等。在混合液中加入2.5mol/L NaOH溶液150mL恰好反应,则原溶液中NO3-的浓度为
A.1.25mol/L B.3.75mol/L C.2.5mol/LD.5.0mol/L
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省豫东、豫北十所名校高三阶段性测试理综化学试卷(解析版) 题型:填空题
【化学——选修2:化学与技术】(15分)
通过海水能获得淡水、食盐、镁等,食盐可进一步用于氯碱工业。请回答下列问题。
(1)列举两种海水淡化的方法:_________、_________。
(2)氯碱工业通过电解饱和食盐水能获得烧碱和氯气等物质,该反应的化学方程式为_____________,如图是用离子交换膜法电解饱和食盐水的原理示意图。其中石墨接电源_________极,电解时铁电极的电极反应式为_________。电解过程中通过离子交换膜的主要离子是__________。

(3)侯氏制碱法中,首先向饱和食盐水中通入CO2和NH3制备NaHCO3,其化学方程式为____________;先通入的是__________(填化学式),其理由是__________________ ;再利用NaHCO3受热分解可制备纯碱。
(4)目前世界上60%以上的镁都是从海水中提取的,已知:MgO和MgCl2的熔点分别为2852℃和714℃。分析说明工业上采用电解熔融MgCl2而不是电解熔融MgO的理由__________ ______________________________________________________________________ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com