
科目:高中化学 来源: 题型:
氢氧燃料电池以KOH溶液为电解质溶液,下列有关该电池的叙述不正确的是
( )
A.正极反应式为:O2+2H2O+4e-===4OH-
B.工作一段时间后,电解液中KOH的物质的量浓度不变
C.该燃料电池的总反应方程式为:2H2+O2===2H2O
D.用该电池电解CuCl2溶液,产生2.24 L Cl2(标准状况)时,有0.4 mol 电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:2CrO42-(黄色)+2H+  Cr2O72-(橙色)+H2O。现以铬酸钾为原料,电化学法制备重铬酸钾的实验装置示意图如下(阳离子交换膜只允许阳离子通过):
Cr2O72-(橙色)+H2O。现以铬酸钾为原料,电化学法制备重铬酸钾的实验装置示意图如下(阳离子交换膜只允许阳离子通过):
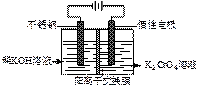
下列说法不正确的是
A.在阴极室,发生的电极反应为:2H2O+2e-=2OH-+H2↑
B.在阳极室,通电后溶液逐渐由黄色变为橙色,是因为产生的H+,与CrO42-离子反应使2CrO42-+2H+  Cr2O72-+H2O向右进行
Cr2O72-+H2O向右进行
C.该制备过程总反应的化学方程式为:
4K2CrO4+4H2O 2K2Cr2O7+4KOH+2H2↑+O2↑
2K2Cr2O7+4KOH+2H2↑+O2↑
D.测定阳极液中K和Cr的含量,若K与Cr的物质的量之比(nK/nCr )为d,则此时铬酸钾的转化率为1-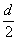
查看答案和解析>>
科目:高中化学 来源: 题型:
用惰性电极电解尿素[CO(NH2)2]的碱性溶液制氢,装置如下图所示,电解池中的隔膜仅阻止气体通过。电解时总的化学方程式为:
CO(NH2)2+2OH-通电CO32-+N2↑+3H2↑
以下说法不正确的是
A.a为阳极,b为阴极
B.电解时,溶液中OH—向b极移动
C.阴极反应式:2H2O+2e-===H2↑+2OH-
D.电解后,溶液pH减小

查看答案和解析>>
科目:高中化学 来源: 题型:
氧化铁在工业上具有广泛的应用。
I.据报道,一定条件下利用Fe2O3与甲烷反应可制取“纳米级”的金属铁。其反应如下:
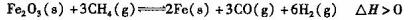
(1)若反应在2L的密闭容器中进行,5min后达到平衡,测得反应生成Fe的质量为l.12g。则该段时间内CH4的平均反应速率为 ________________ 。
(2)反应达到平衡后,保持其他条件不变,仅改变某一相关元素,下列说法正确的是 ________________(选填序号)。
a.若加入催化剂,v正增大,平衡向右移动
b.若温度升高,平衡常数K减小
c.若增大Fe2O3的量,平衡向右移动
d.若从反应体系中移走部分CO,可提高CH4的转化率
Ⅱ.工业上利用硫铁矿烧渣(主要成分为Fe2O3、A12O3、SiO2等)为原料提取Fe2O3,工艺 流程如下:试回答下列问题:
流程如下:试回答下列问题:
(3)结合下图,判断步骤ⅱ中调节溶液的pH范围_________________。
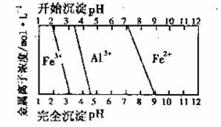
(4)写出步骤2中发生反应的离子方程式_____________________________,步骤2中分离出的滤渣的化学式是_________________。
(5)已知

 计算 的平衡常数为_____。
计算 的平衡常数为_____。
(6)在空气中煅烧FeCO3生成氧化铁的化学方程式为____________。
(7)结合所学化学知识,请你设计在实验室里从上述的硫铁矿烧渣中提取氧化铁的另一种简单方案_________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
醋酸和氢氧化钠溶液发生反应的离子方程式正确的是
A.H++OH-→H2O B.H++ NaOH→Na++H2O
C.CH3COOH +OH-→CH3COO- +H2O D.CH3COOH + NaOH→CH3COO-+ Na++H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
氧化还原反应在生产、生活中具 有广泛的用途。下列做法中涉及到铝元素的还原性的是
有广泛的用途。下列做法中涉及到铝元素的还原性的是
A.明矾净化水
B.用氢氧化铝治疗胃酸过多
C.用铝制容器存放浓硫 酸
酸
D.电解熔融氧化铝制单质铝
查看答案和解析>>
科目:高中化学 来源: 题型:
硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组的同学欲测定该补血剂中铁元素的含量。实验步骤如下:

请回答下列问题:
(1)证明步骤①滤液中含有Fe2+的方法是:取样,先滴加KSCN溶液,再滴加________,该过 程的现象为:_____________________________________________________________。
程的现象为:_____________________________________________________________。
(2)步骤②加入过量H2O2的目的是:______________________________________。
(3)步骤③中反应的离子方程式是:_______________________________________。
(4)步骤④中一系列处理的操作步骤:过滤、________、灼烧、________、称量。
(5)若实验中铁无损耗,则每片补血剂中含铁元素的质量为________ g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com