
已知反应X+Y=M+N为吸热反应,对这个反应的下列说法中正确的是( )
A.X的能量一定低于M的,Y的能量一定低于N的
B.因为该反应为吸热反应,故一定要加热反应才能进行
C.破坏反应物中的化学键所吸收的能量小于形成生成物中化学键所放出的能量
D.X和Y的总能量一定低于M和N的总能量
科目:高中化学 来源:2015-2016学年天津市高一下期中化学试卷(解析版) 题型:填空题
W、X、Y、Z、M、G五种短周期元素,原子序数依次增大。W,Z同主族,可形成离子化合物ZW;Y , M同主族,可形成MY2, MY3两种分子;X的气态氢化物水溶液呈碱性。
请回答下列问题:
(1)Y在元素周期表中的位置为 ;
(2)上述五种元素的最高价氧化物对应的水化物酸性最强的是 (写化学式)
(3) W、Y、Z、G形成的简单离子的半径大小顺序是 (用化学符号表示)
(4)Y、G的单质或两元素之间形成的化合物可作水消毒剂的有 (任写两个)
(5)Y与M的氢化物中,热稳定性差的是 (填化学式),沸点高的是 (填化学式)
(6)ZW的电子式为 ,W2Y2的电子式为 ,用电子式表示Z2M的形成过程: 。
(7)MY2和G2均能使品红溶液褪色,常温常压下若将相同体积的MY2和G2气体同时通入品红溶液,品红溶液 (填“褪色”或“不褪色”),请用相关离子方程式解释原因 。
(8)已知
化合物 | MgO | Al2O3 | MgCl2 | AlCl3 |
类型 | 离子化合物 | 离子化合物 | 离子化合物 | 共价化合物 |
熔点/℃ | 2800 | 2050 | 714 | 191 |
工业制镁时,电解MgCl2而不电解MgO的原因是是 ;制铝时,电解Al2O3而不电解AlCl3的原因是 。
(9)最近意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的N4分子。N4分子结构如下图所示,已知断裂1 mol N—N吸收167 kJ热量,生成1 mol N≡N入出942kJ。根据以上信息和数据,下列说法正确的是 。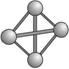
A.N4属于一种新型化合物 B.N4晶体熔点高,硬度大
C.相同质量的N4的能量高于N2 D.1molN4转变为N2将吸收882kJ的能量.
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高一下期中化学试卷(解析版) 题型:选择题
下表是元素周期表的一部分,下列有关说法的组合中正确的是
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA |
2 | a | b | |||||
3 | d | e | f | g | h | i |
①a、b、e、f四种元素的原子半径:e > f > b > a
②h、i两种元素阴离子的还原性:h > i
③a、g两种元素氢化物的稳定性:a > g
④d、e、f三种元素最高价氧化物对应水化物的碱性依次增强
⑤八种元素中d元素的单质还原性最强,i元素的单质氧化性最强
A.①③④ B.②③⑤ C.②④⑤ D.①③⑤
查看答案和解析>>
科目:高中化学 来源:2015-2016学年宁夏育才中学高一下期中化学试卷(解析版) 题型:填空题
下图是元素周期表的一部分,表中的①~⑩中元素,用元素符号或化学式填空回答:
族 周 期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
二 | ① | ② | ||||||
三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
四 | ⑨ | ⑩ |
(1)在这些元素中,化学性质最不活泼的原子的原子结构示意图为 [
(2)地壳中含量最多的金属元素的名称是
(3)用电子式表示②与④形成化合物的过程 。
(4)这些元素中的最高价氧化物对应的水化物中,酸性最强的是 (用化学式作答,下同),碱性最强的是 。
(5)写出⑤与氢氧化钠反应的化学方程式: 。写出⑤的氢氧化物与氢氧化钠溶液反应的离子方程式: 。
(6)②和⑥,②和⑨形成的化合物含有的化学键类型分别是 ,
查看答案和解析>>
科目:高中化学 来源:2015-2016学年宁夏育才中学高一下期中化学试卷(解析版) 题型:选择题
碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌—锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:Zn(s)+2MnO2(s)+H2O(l)=Zn(OH)2(s)+Mn2O3(s) ,下列说法错误的是( )
A.电池工作时,锌失去电子
B.电池正极得电子反应产物是Mn2O3(s)
C.电池工作时,电子由正极通过外电路流向负极
D.外电路中每通过O.2mol电子,锌的质量理论上减小6.5g
查看答案和解析>>
科目:高中化学 来源:2015-2016学年宁夏育才中学高一下期中化学试卷(解析版) 题型:选择题
下列事实能判断金属元素甲的金属性一定比乙强的有( )
①甲单质能与乙盐的溶液反应并置换出乙
②甲、乙两元素原子的最外层电子数相同,且甲的原子半径小于乙
③甲、乙两短周期元素原子的电子层数相同,且甲的原子序数小于乙
④甲、乙两元素的最高价氧化物水化物的碱性甲大于乙
A.全部可以 B.仅②可以 C.仅②③可以 D.①③④可以
查看答案和解析>>
科目:高中化学 来源:2015-2016学年宁夏育才中学高一下期中化学试卷(解析版) 题型:选择题
下列关于F、Cl、Br、I性质的比较,不正确的是( )
A.它们的原子半径、失电子能力随核电荷数的增加而增大
B.被其它卤素单质从其卤化物中置换出来的可能性随核电荷数的增加而增大
C.它们的氢化物的稳定性随核电荷数的增加而增强
D.单质的颜色随核电荷数的增加而加深
查看答案和解析>>
科目:高中化学 来源:2016届陕西省高三第六次适应性考试理综化学试卷(解析版) 题型:实验题
氢化镁(MgH2)是一种相对廉价的储氢材料,遇水易发生反应,在潮湿空气中能自燃。某兴趣小组拟选用如下装置制备氢化镁。
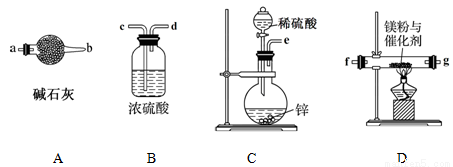
请回答下列问题:
(1)实验装置中,按气体流向的依次连接合理顺序为____________________(填仪器接口处的字母编号)。
(2)用连接好的实验装置进行实验,实验步骤如下:检查装置气密性后,装入药品;打开分液漏斗活塞, (用编号按正确的顺序排列下列步骤)。
①关闭分液漏斗活塞 ②收集气体并检验纯度
③加热反应一段时间 ④停止加热,充分冷却
(3)为了确认进入装置D中的氢气已经干燥,可在D装置前面再加一个装置,该装置中加入的试剂的名称是 。
(4)通过上述方法制得的氢化镁样品中常混有未完全反应的镁和其他杂质,假设样品中的氢化镁与水完全反应,而镁粉和其他杂质均不与水反应)。测定实验样品纯度的方法步骤如下:
Ⅰ.检查装置气密性,装入药品,按下图(固定装置省略)所示连接仪器。
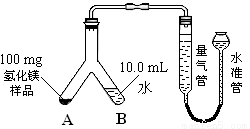
Ⅱ.调整水准管高度,使量气装置两边的液面保持同一水平。读取液面所在的刻度数据为10.0 mL。
Ⅲ.将Y形管慢慢倾斜,直到B端的水全部与A端的样品混合。
Ⅳ.反应结束,冷却至室温,再次读取液面所在刻度数据为128.0 mL。
回答下列问题:
①第Ⅳ步骤在读取量气管中数据时,若发现水准管中的液面低于量气管中液面,应采取的措施是 。
②反应生成氢气的体积为 mL。
③已知该实验条件下,氢气的密度为0.09 mg/mL。样品中氢化镁的纯度为 (结果精确到0.01%)。
(5)请你设计一个定性实验,鉴别镁粉与氢化镁粉末(不可使用水),写出实验的简要步骤、现象及结论 。
查看答案和解析>>
科目:高中化学 来源:2016届江西南昌二中、临川一中等高三4月联考二理综化学试卷(解析版) 题型:选择题
用下列实验装置进行相应实验,装置正确且能达到实验目的的是
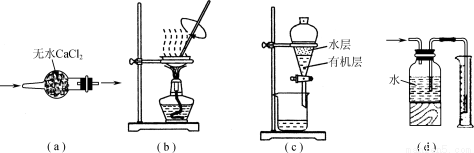
A.用图a所示装置干燥SO2气体
B.用图b所示装置蒸发CH3COONa溶液得醋酸钠晶体
C.用图c所示装置分离有机层与水层,水层从分液漏斗下口放出
D.用图d所示装置测量氯气的体积
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com