
| A.CO2、PbO2都是强氧化剂 |
| B.CO2和PbO2都是弱氧化剂,CO和PbO都是还原剂 |
| C.Sn(OH)4可与NaOH反应,但不与盐酸反应 |
| D.Ge单质的熔点介于Si、Pb之间,是半导体材料 |
科目:高中化学 来源:不详 题型:单选题
| A.二氧化硅晶体是一种具有立体网状结构的原子晶体 |
| B.二氧化硅不溶于水,也不跟水起反应生成酸 |
| C.二氧化硅是一种酸性氧化物,它不跟任何酸起反应 |
| D.二氧化硅与二氧化碳在物理性质上有很大差异 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.50、0.50、0.50 | B.0.50、1.0、1.5 | C.0.25、1.0、1.5 | D.1.0、0.25、0.17 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.硅的非金属性比碳的活泼 |
| B.二氧化硅中硅氧键的类型和二氧化碳中碳氧键不同 |
| C.硅氧键的键能比碳氧键的键能大得多 |
D.二氧化硅晶体类型和二氧化碳晶体不同        |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
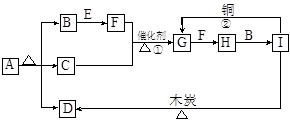
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
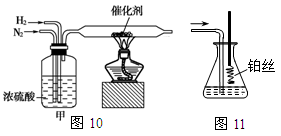
| A.浓硝酸通常保存在棕色的试剂瓶中,说明浓硝酸不稳定 |
| B.足量铁与稀硝酸反应后溶液呈浅绿色,说明稀硝酸不能氧化亚铁离子 |
| C.不用浓硝酸与铜屑反应来制取硝酸铜,说明浓硝酸具有挥发性 |
| D.不用锌与稀硝酸反应制取氢气,说明稀硝酸能将锌钝化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
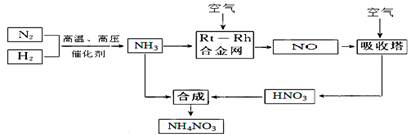
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
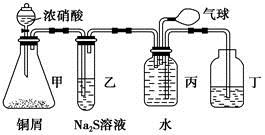
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com