
【题目】在恒温恒容的密闭容器中按照下表甲、乙、丙三种方式分别投料,发生反应:3H2(g)+N2(g) ![]() 2NH3(g),测得甲容器中H2的平衡转化率为 40%,下列说法正确的是( ).
2NH3(g),测得甲容器中H2的平衡转化率为 40%,下列说法正确的是( ).
N2(mol) | H2(mol) | NH3(mol) | |
甲 | 1 | 3 | 0 |
乙 | 0.5 | 1.5 | 1 |
丙 | 0 | 0 | 4 |
A.乙容器中反应向逆向进行
B.达到平衡时,甲、乙、丙三容器中NH3体积分数的大小顺序:甲=乙>丙
C.乙中的NH3转化率为40%
D.若丙在恒温恒压的密闭容器进行,平衡后往容器中再充入4 mol NH3,重新达到平衡时,体系中NH3体积分数不变
【答案】AD
【解析】
A. 甲、乙容器是等效的, ,根据甲中氨气的量为0.8mol,则乙中反应向逆向进行,故A正确;
,根据甲中氨气的量为0.8mol,则乙中反应向逆向进行,故A正确;
B. 达到平衡时,甲、乙两个容器中NH3体积分数的大小相等:甲=乙,丙容器可以理解先变为是甲容器的两倍,则此时NH3体积分数与甲相等,但又变为与甲容器一样大,则加压,平衡正向移动,氨气体积分数变大,因此三个容器中NH3体积分数的大小相等:丙>甲=乙,故B错误;
C. 甲乙容器是等效平衡的,平衡是氨气的物质的量为0.8mol,乙则消耗0.2mol,此时乙中的NH3转化率![]() ,故C错误;
,故C错误;
D. 若丙在恒温恒压的密闭容器进行,平衡后往容器中再充入4 mol NH3,前后两者是等效平衡,重新达到平衡时,体系中NH3体积分数不变,故D正确。
综上所述,答案诶AD。


 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案科目:高中化学 来源: 题型:
【题目】下列化学用语,应用正确的是 ( )
A.硝基苯的结构简式是:![]()
B.乙炔的电子式是:![]()
C.乙醚分子的球棍模型是:
D.甲酸中存在一CHO和—COOH两种官能团
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有三份不同质量的硫化铜与硫化亚铜的混合物样品①②③。甲、乙、丙三同学各取一种样品,加强热充分反应,测定各样品中硫化铜的量。
(1)甲取2.56克样品①,置于空气中加强热,产物为氧化铜和二氧化硫。若产生0.448 L气体(标准状况),该气体被30 mL一定浓度氢氧化钠恰好完全吸收,将所得溶液小心低温蒸干得固体2.3克。则样品①中硫化铜的质量为_____g,氢氧化钠浓度_______mol·L-1;
(2)乙取3.52克样品②,投入过量的浓硝酸中加热,充分反应后,样品全部参与反应,溶液失重8.44克。样品②中硫化铜的物质的量为____mol;若浓硝酸的浓度为14.2 mol·L-1,则反应消耗浓硝酸____mL。(已知:Cu2S+14HNO3→2Cu(NO3)2+10NO2↑+H2SO4+6H2O)
(3)丙称量样品③强热后剩余的固体质量比原样品减小了a g,若该固体为氧化铜,则样品③中硫化铜物质的量(n)为_________mol。若要计算硫化亚铜的质量,则缺少_____________数据,若设该数据为b克,则硫化亚铜的质量为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列物质变化,所得能量变化关系正确的是
物质变化 | 能量关系 | |
A | 将充满NO2的针筒置于热水中,气体颜色变深 | 1molN2O4(g)的能量>2molNO2(g)的能量 |
B | 将NaOH溶液与HCl溶液混合 |
|
C | 1g气态SiH4在空气中燃烧,生成SiO2 (s)与液态水,放热44.6kJ | SiH4(g)+2O2(g)→SiO2(s)+2H2O(l)+44.6kJ |
D | 合成氨:N2(g)+3H2(g) | 反应物的总键能>生成物的总键能 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】交通运输部在南海华阳礁举行华阳灯塔和赤瓜灯塔竣工发光仪式,宣布两座大型多 功能灯塔正式发光并投入使用。镁-海水电池可为灯塔提供能源,其装置如图所示。下列有关镁-海水电池的说法正确的是( ).
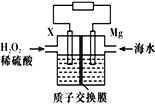
A.镁被还原
B.该电池工作一段时间后,左侧溶液质量减轻
C.正极的电极反应式为H2O2+2e-+2H+=2H2O
D.若电池工作时,SO42-从交换膜左侧向右侧迁移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列描述不正确的是( ).
A.在滴有酚酞的 Na2CO3溶液中慢慢滴入BaCl2溶液至过量,溶液的红色褪去
B.往Na2CO3溶液中加水,![]() 增大
增大
C.pH相同的①NH4Cl、②NH4Al (SO4)2、③NH4HSO4三种溶液中c(NH4+):①>②>③
D.在水电离出的c(H+)=1×10-12 mol/L的溶液中,Al3+一定不可能大量存在
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】滴定法不仅适合于酸碱中和滴定,还可以用于氧化还原滴定和沉淀滴定。
I. 甲同学根据反应:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O,进行测定H2C2O4溶液的物质的量浓度的实验。实验步骤如下:
①取待测H2C2O4溶液25.00 mL放入锥形瓶中,再加入适量的稀硫酸;
②用0.1 mol/L KMnO4溶液滴定至终点,记录数据;
③重复滴定2次,平均消耗KMnO4溶液20.00 mL。请回答:
(1)滴定时,将KMnO4溶液装在 __________(填“酸式”或“碱式”)滴定管中。
(2)滴定过程中眼睛注视 __________。
(3)计算H2C2O4溶液的物质的量浓度为 ________mol/L。
(4)在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有 _________(填字母代))。
A 滴定终点读数时俯视 B 取用待测液的滴定管水洗后未用待测液润洗
C 锥形瓶水洗后未干燥 D 装标准液的滴定管尖嘴部分有气泡,滴定后消失
II. 已知:
AgCl | AgBr | AgSCN | Ag2CrO4 | AgCN | |
溶解度(mol/L) | 1.34×10-6 | 7.1×10-7 | 1.0×10-6 | 6.5×10-5 | 1.1×10-8 |
颜色 | 白 | 淡黄 | 白 | 砖红 | 白 |
(5)①乙同学参照上表已知信息用硝酸银标准溶液滴定氯离子含量时可以作指示剂的是_______(填字母代号)。
a CaCl2 b NaBr c NaCN d K2CrO4
②滴定达终点的现象是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO、CO2的应用和治理是当今社会的热点问题。CO工业上可用于高炉炼铁,发生如下反应:1/3Fe2O3(s)+CO(g)2/3Fe(s)+CO2(g),已知该反应在不同温度下的平衡常数如表:

(1)该反应的正反应为_______反应(填“放热”或“吸热”),欲提高CO的平衡转化率,促进Fe2O3的转化,可采取的措施是___________(选填序号)
a、及时吸收或移出CO2 b、增大反应体系的压强。
c、使用更高效的催化。 d、粉碎矿石增大接触面积
(2)一定条件下,在容积一定的容器中,铁和CO2发生反应:2Fe (s) +CO2 (g)FeO(s) +CO (g) –Q,该反应的平衡常数表达式K=____________。下列措施中能使平衡时c(CO)/c(CO2)增大的是___________(选填编号)。
a.升高温度 b.增大压强
c.充入一定量一氧化碳在 d.再加入一些铁粉
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组为研究电化学原理,设计如图装置。下列叙述不正确的是

A. a和b不连接时,铁片上会有金属铜析出
B. a和b用导线连接时,铜片上发生的反应为:Cu2++2e-= Cu
C. 无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿色
D. a和b分别连接直流电源正、负极,电压足够大时,Cu2+向铜电极移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com