
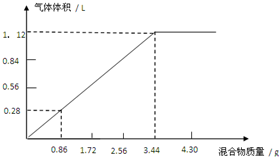
 在硝酸铵和硫酸铵的固体混合物中加入50mL NaOH溶液,充分加热反应,混合的质量与产生的气体的体积如图所示.
在硝酸铵和硫酸铵的固体混合物中加入50mL NaOH溶液,充分加热反应,混合的质量与产生的气体的体积如图所示.
| ||
| V |
| Vm |
| n |
| V |
| ||
| 1.12L |
| 22.4L/mol |
| 0.05mol |
| 0.05L |
| 1×10-14 |
| 1 |
| 1.12L |
| 22.4L/mol |
| 14g/mol×0.06mol |
| 3.44g |


 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、240 mL 0.2 mol?L-1的NaCl溶液配制:需要使用天平、250 mL容量瓶等仪器 |
| B、向FeCl3稀溶液中滴加NaOH溶液,并加热煮沸,可制备Fe(OH)3胶体 |
| C、不慎将NaOH溶液溅到皮肤上,应立即用较多的水冲洗 |
| D、用苯萃取碘水中的碘时,萃取后的油层不能从分液漏斗下端放出 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用蒸馏水冼净滴定管后,即装入标准盐酸进行滴定 |
| B、用蒸馏水冼净锥形瓶后,再用NaOH液润洗,而后装入一定体积的NaOH溶液 |
| C、用碱式滴定管取10.00mLNaOH溶液放入洁净的锥形瓶中,再加入适量蒸馏水后进行滴定 |
| D、改用量筒量取10.0mLNaOH溶液,放入锥形瓶后进行滴定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
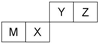
| A、X 的最简单气态氢化物的热稳定性比Z的小 |
| B、Z位于元索周期表中第2周期、第ⅥA族 |
| C、原子半径Z<M |
| D、Y的最高价氧化物对应水化物的酸性比X 的弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com