
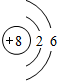 £¬BµÄĄė×Ó½į¹¹Ź¾ŅāĶ¼
£¬BµÄĄė×Ó½į¹¹Ź¾ŅāĶ¼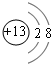 £¬DµÄµ„ÖŹ·Ö×ӵĵē×ÓŹ½
£¬DµÄµ„ÖŹ·Ö×ӵĵē×ÓŹ½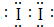 £®
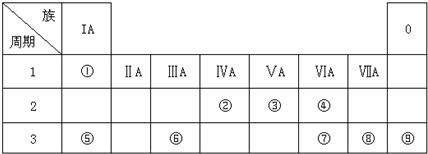
£®·ÖĪö ĻÖÓŠA”¢B”¢C”¢D”¢EĪåÖÖŌŖĖŲ£¬ĖüĆĒµÄÖŹ×ÓŹżŅĄ“ĪŌö¶ą£®¢ŁAµÄŗĖµēŗÉŹż“óÓŚ2£¬æÉŠĪ³ÉĒā»ÆĪļH2A£¬øĆĒā»ÆĪļµÄ³£ĪĀĻĀŹĒŅŗĢ壬ŌņAĪŖOŌŖĖŲ£¬Ēā»ÆĪļĪŖH2O£»¢ŚAŗĶBĮ½ŌŖĖŲæÉŠĪ³ÉB2A3»ÆŗĻĪļ£¬øĆ»ÆŗĻĪļ¼ČÄÜČÜÓŚĒæĖį£¬ÓÖÄÜČÜÓŚĒæ¼ī£¬ŌņBĪŖAl£¬ŠĪ³ÉµÄ»ÆŗĻĪļĪŖAl2O3£»¢ŪC+Ąė×Ó±ČB3+Ąė×Ó¶ą8øöµē×Ó£¬ŌņCĪŖKŌŖĖŲ£»¢ÜCÓėDŌŖĖŲæÉŅŌŠĪ³É»ÆŗĻĪļCD£¬¢ŻCDµÄČÜŅŗÖŠĶØČėĀČĘųŗó¼Óµķ·ŪČÜŅŗĻŌĄ¶É«£¬ŌņDĪŖIŌŖĖŲ£»¢ŽE”¢CĶ¬Ö÷×壬ĒŅE±ČC¶ąĮ½øöµē×Ó²ć£¬Eµ„ÖŹæÉÓėĄäĖ®·“Ӧɜ³ÉĒāĘų£¬ŌņEĪŖCs£®
½ā“š ½ā£ŗĻÖÓŠA”¢B”¢C”¢D”¢EĪåÖÖŌŖĖŲ£¬ĖüĆĒµÄÖŹ×ÓŹżŅĄ“ĪŌö¶ą£®¢ŁAµÄŗĖµēŗÉŹż“óÓŚ2£¬æÉŠĪ³ÉĒā»ÆĪļH2A£¬øĆĒā»ÆĪļµÄ³£ĪĀĻĀŹĒŅŗĢ壬ŌņAĪŖOŌŖĖŲ£¬Ēā»ÆĪļĪŖH2O£»¢ŚAŗĶBĮ½ŌŖĖŲæÉŠĪ³ÉB2A3»ÆŗĻĪļ£¬øĆ»ÆŗĻĪļ¼ČÄÜČÜÓŚĒæĖį£¬ÓÖÄÜČÜÓŚĒæ¼ī£¬ŌņBĪŖAl£¬ŠĪ³ÉµÄ»ÆŗĻĪļĪŖAl2O3£»¢ŪC+Ąė×Ó±ČB3+Ąė×Ó¶ą8øöµē×Ó£¬ŌņCĪŖKŌŖĖŲ£»¢ÜCÓėDŌŖĖŲæÉŅŌŠĪ³É»ÆŗĻĪļCD£¬¢ŻCDµÄČÜŅŗÖŠĶØČėĀČĘųŗó¼Óµķ·ŪČÜŅŗĻŌĄ¶É«£¬ŌņDĪŖIŌŖĖŲ£»¢ŽE”¢CĶ¬Ö÷×壬ĒŅE±ČC¶ąĮ½øöµē×Ó²ć£¬Eµ„ÖŹæÉÓėĄäĖ®·“Ӧɜ³ÉĒāĘų£¬ŌņEĪŖCs£®
£Ø1£©ÓÉÉĻŹö·ÖĪöæÉÖŖ£¬CĪŖ¼Ų£¬EĪŖļ¤£¬
¹Ź“š°øĪŖ£ŗ¼Ų£»ļ¤£»
£Ø2£©AĪŖOŌŖĖŲ£¬Ō×Ó½į¹¹Ź¾ŅāĶ¼ĪŖ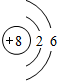 £¬BĪŖAl£¬Ąė×Ó½į¹¹Ź¾ŅāĶ¼ĪŖ
£¬BĪŖAl£¬Ąė×Ó½į¹¹Ź¾ŅāĶ¼ĪŖ £¬DµÄµ„ÖŹĪŖI2£¬·Ö×ӵĵē×ÓŹ½ĪŖ
£¬DµÄµ„ÖŹĪŖI2£¬·Ö×ӵĵē×ÓŹ½ĪŖ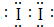 £¬
£¬
¹Ź“š°øĪŖ£ŗ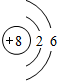 £»
£» £»
£»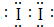 £»
£»
£Ø3£©Al2O3·Ö±šÓėŃĪĖįŗĶĒāŃõ»ÆÄĘČÜŅŗ·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗAl2O3+6H+=2Al3++3H2O”¢Al2O3+2OH-=2AlO2-+H2O£¬
¹Ź“š°øĪŖ£ŗAl2O3+6H+=2Al3++3H2O£»Al2O3+2OH-=2AlO2-+H2O£»
£Ø4£©Ąė×Óµē×Ó²ćŌ½¶ąĄė×Ó°ė¾¶Ō½“󣬹ŹĄė×Ó°ė¾¶£ŗCs+£¾K+£¾Al3+£¬½šŹōŠŌŌ½Ē棬ŃōĄė×ÓŃõ»ÆŠŌŌ½Čõ£¬¹ŹŃõ»ÆŠŌ£ŗAl3+£¾K+£¾Cs+£¬
¹Ź“š°øĪŖ£ŗCs+£¾K+£¾Al3+£»Al3+£¾K+£¾Cs+£»
£Ø5£©ļ¤ÓėĄäĖ®·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ2Cs+2H2O=2CsOH+H2”ü£¬
¹Ź“š°øĪŖ£ŗ2Cs+2H2O=2CsOH+H2”ü£®
µćĘĄ ±¾Ģāæ¼²é½į¹¹ŠŌÖŹĪ»ÖĆ¹ŲĻµÓ¦ÓĆ£¬ĶʶĻŌŖĖŲŹĒ½āĢā¹Ų¼ü£¬²ąÖŲ¶Ō»ÆѧÓĆÓļ”¢ŌŖĖŲ»ÆŗĻĪļÖŖŹ¶µÄ漲飬עŅā¶Ō»ł“”ÖŖŹ¶µÄČ«ĆęÕĘĪÕ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ·Ö×ÓŹ½·ūŗĻCnH2n+2µÄĢžŅ»¶ØŹĒĶéĢž | |
| B£® | ĶéĢž¾łÄÜÓėĀČĖ®·¢ÉśČ”“ś·“Ó¦ | |
| C£® | ÕżĪģĶéµÄČŪ·Šµć±ČŅģĪģĶéµÄøß | |
| D£® | ĶéĢž²»Äܱ»ĖįŠŌøßĆĢĖį¼ŲµČĒæŃõ»Æ¼ĮŃõ»Æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | äå±½ÖŠŗ¬ÓŠäåµ„ÖŹ£¬æÉÓĆNaOHČÜŅŗĻ“µÓ£¬ŌŁ¾·ÖŅŗ¶ų³żČ„ | |
| B£® | Ļõ»ł±½ÖŠ»ģÓŠµÄĮņĖįŗĶĻõĖįæÉÓĆNaOHČÜŅŗĻ“µÓ£¬ŌŁ¾·ÖŅŗ¶ų³żČ„ | |
| C£® | ±½ÖŠµÄÉŁĮæ±½·ÓæÉÓĆNaOHČÜŅŗĻ“µÓ£¬ŌŁ¾·ÖŅŗ¶ų³żČ„ | |
| D£® | ±½ÖŠµÄÉŁĮæ±½·ÓæɼÓČėÅØäåĖ®£¬ŌŁ¾¹żĀĖ¶ų³żČ„ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 56 | B£® | 158 | C£® | 258 | D£® | 101 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ś¢Ū¢Ü¾łæÉ | B£® | Ö»ÓŠ¢Ł¢Ś¢Ü | C£® | Ö»ÓŠ¢Ś¢Ū¢Ü | D£® | Ö»ÓŠ¢Ū¢Ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | ČÜŅŗÖŠµÄŃōĄė×ÓŅĘĻņÕż¼« | |
| B£® | øŗ¼«·“Ó¦Ź½£ŗCH3OH+8OH--6e-ØTC+6H2O | |
| C£® | µē³ŲŌŚŹ¹ÓĆ¹ż³ĢÖŠ£¬µē½āÖŹČÜŅŗµÄc£ØOH-£©²»±ä | |
| D£® | µ±ĶāµēĀ·Ķعż6 molµē×ÓŹ±£¬ĄķĀŪÉĻĻūŗÄ1.5 mol O2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CH2CH2OH | B£® | 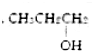 | C£® | 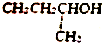 | D£® | 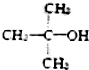 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com