
在硫酸铝、硫酸钾和明矾[KAl(SO4)2·12H2O]的混合溶液中,SO42—的浓度为0.4mol/L,当加入等体积0.4mol/L KOH溶液时,生成的沉淀恰好完全溶解。则反应后溶液中K+的浓度约为
| A.0.225mol/L | B.0.25mol/L | C.0.45mol/L | D.0.9mol/L |
C
解析试题分析:设体积均为1L,铝离子的物质的量是x。由于生成沉淀完全溶解,所以反应为
Al3++4OH-=AlO2-+2H2O
1 4
x 0.4mol
即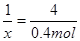
解得x=0.1mol
即含有0.1molAl3+
原溶液中只含有K+,Al3+和SO42-,根据电荷守恒
则n(K+)+3n(Al3+)=2n(SO42-)
而n(Al3+)=0.1mol,n(SO42-)=0.4mol
所以n(K+)+3×0.1mol=2×0.4mol
解得n(K+)=0.5mol
而反应时KOH又引入了0.4molK+
所以K+总量为0.9mol
此时溶液体积变为2L
故c(K+)=0.45mol/L,故选:C。
考点:考查有关混合物的计算


 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:实验题
对实验过程中出现的异常现象进行探究,是实施素质教育、培养创新精神的有效途经。
【实验1】用下图实验装置进行铜与浓硫酸的反应,实验中发现试管内除了产生白色硫酸铜固体外,在铜丝表面还有黑色固体甲生成,甲中可能含有黑色的CuO、CuS、Cu2S。查阅资料:CuS和Cu2S均为黑色固体,常温下都不溶于稀盐酸,在空气中煅烧,均转化为CuO和SO2。为了探究甲的成分,该小组同学在收集到足够量的固体甲后,进行了如下实验:

(1)上述实验装置除了有尾气吸收装置外,还有一个显著的优点是 。
(2)固体乙在空气中煅烧时,使用的实验仪器除了玻璃棒、三脚架、酒精灯外,还必须有 。
(3)确定乙是否煅烧完全的操作是 。
(4)煅烧过程中一定发生的化学反应方程式为 。
【实验2】某化学兴趣小组设计了如下实验装置(尾气吸收装置未画出),探究Cl2、Br2、Fe3+的氧化性强弱。
(5)根据下列实验操作和现象,填写实验结论。
| 实验操作 | 实验现象 | 结论 |
| 打开活塞a,向圆底烧瓶中滴入适量浓盐酸;然后关闭活塞a,点燃酒精灯。 | D装置中:溶液变红 E装置中:水层溶液变黄, 振荡后,CCl4层无明显变化。 | Cl2、Br2、Fe3+的氧化性由强到弱的顺序为: |
| ⅰ.(SCN)2性质与卤素单质类似。氧化性:Cl2>(SCN)2。 ⅱ.Cl2和Br2反应生成的BrCl呈红色,沸点约5℃,与水发生水解反应。 ⅲ.AgClO、AgBrO均可溶于水。 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
将一定质量的铁、氧化铁、氧化铜的混合物粉末放入100mL 4.40 mol/L盐酸中,充分反应后产生896 mL H2(标准状况),残留固体1.28g。过滤,滤液中无Cu2+。将滤液加水稀释到200mL,测得其中c(H+)为0.400mol/L。则原混合物中单质铁的质量是
| A.2.24g | B.3.36g | C.5.60g | D.10.08g |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
氧化亚铁粉末和铝粉配成铝热剂,分成两等份。一份在高温下恰好完全反应后,在与盐酸反应;另一份直接放入足量的烧碱溶液中充分反应。前后两种情况下生成的气体的质量比是
A.1:1 B.2:3 C. 3:2 D 28:9
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列解释事实的方程式不准确的是
| A.铝热法炼铁:Fe2O3 + 2Al高温 Al2O3 + 2Fe |
B.工业上用NH3制备NO:4NH3 + 5O2 4NO + 6H2O 4NO + 6H2O |
| C.向受酸雨影响的湖泊中喷洒CaCO3粉末:CO32- + 2H+="=" H2O + CO2↑ |
| D.过氧化钠用于呼吸面具中作为氧气的2Na2O2 + 2CO2 ==2Na2CO3 + O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
将一定质量的Mg和Al的混合物投入500mL稀硫酸中,固体全部溶解并产生气体。待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示。则下列说法正确的是( ) 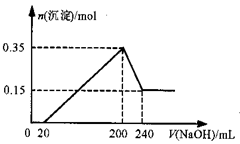
| A.Mg和Al的总质量为8g |
| B.硫酸的物质的量浓度为5 mol/L |
| C.生成的H2在标准状况下的体积为11.2L |
| D.NaOH溶液的物质的量浓度为5mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法不正确的是( )
| A.干燥的氯气可以用钢瓶运输 | B.钠可以保存在CCl4液体中 |
| C.Na2O2可作为潜水艇的供氧剂 | D.实验后剩余的钠粒可放回原试剂瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列物质的转化在给定条件下能实现的是
①SiO2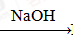 Na2SiO3
Na2SiO3 H2SiO3 ②Fe
H2SiO3 ②Fe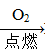 Fe2O3
Fe2O3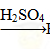 Fe2(SO4)3
Fe2(SO4)3
③BaSO4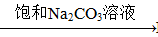 BaCO3
BaCO3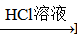 BaCl2 (Ksp(BaSO4)=1.1×10-10 Ksp(BaCO3)=2.6×10-9)
BaCl2 (Ksp(BaSO4)=1.1×10-10 Ksp(BaCO3)=2.6×10-9)
④AlCl3溶液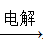 Al
Al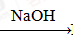 NaAlO2
NaAlO2
⑤HCHO HCOOH
HCOOH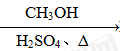 HCOOCH3
HCOOCH3
| A.①②⑤ | B.②③④ | C.②④⑤ | D.①③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
向盛有一定量氢氧化钠溶液的烧杯中通入标准状况下448mL氮气和二氧化碳的混合气体后得到溶液A,在溶液A中逐滴加入0.1mol/L的稀盐酸至过量,并将溶液加热,产生的二氧化碳气体的物质的量与加入稀盐酸的体积的关系如图所示
(忽略二氧化碳的溶解和氯化氢的挥发).下列说法正确的是
| A.原混合气体中氮气与二氧化碳体积之比为1:4 |
| B.在逐滴加入稀盐酸产生二氧化碳之前,发生的离子反应为CO32-+H+═HCO3- |
| C.溶液A中含有0.01molNaOH和0.01molNa2CO3 |
| D.当加入0.1L稀盐酸时,此时溶液中离子浓度大小关系为 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com