
| A. | 盐酸与NaOH溶液反应 | B. | 碳酸氢铵受热分解 | ||
| C. | 铝粉与MnO2反应 | D. | 氧化钙溶于水 |
分析 生成物总能量高于反应物总能量的反应属于吸热反应,根据常见的放热反应和吸热反应进行判断.若反应物的总能量大于生成物的总能量则为放热反应.
常见的放热反应有:所有的物质燃烧、所有金属与酸、所有中和反应、绝大多数化合反应,铝热反应;
常见的吸热反应有:个别的化合反应(如C和CO2)、绝大数分解反应、少数分解置换以及某些复分解(如铵盐和强碱),
A.中和反应都是放热反应,生成物的总能量小于反应物的总能量;
B.大多数分解反应是吸热反应,生成物的总能量大于反应物的总能量;
C.铝粉和二氧化锰是铝热反应属于放热反应,生成物的总能量小于反应物的总能量;
D.氧化钙溶于水与水发生化合反应,属于放热反应,生成物的总能量小于反应物的总能量;
解答 解:A.酸碱中和反应都是放热反应,生成物的总能量小于反应物的总能量,故A不符合;
B.碳酸氢铵分解是吸热反应,生成物的总能量大于反应物的总能量,故B符合;
C.铝粉和二氧化锰属于放热反应,生成物的总能量小于反应物的总能量,故C不符合;
D.氧化钙溶于水与水发生化合反应,属于放热反应,生成物的总能量小于反应物的总能量,故D不符合;
故选B.
点评 本题主要考查了放热反应和放热反应,题目难度不大,掌握常见的放热反应和放热反应是解题的关键.


 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | X可用作木材防火剂 | |
| B. | 步骤II的反应是Na2SiO3+H2SO4═H2SiO3(胶体)+Na2SO4 | |
| C. | 步骤Ⅱ中的稀硫酸可用CO2来代替 | |
| D. | 步骤Ⅲ若在实验室完成,一般在蒸发皿中进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 操作和现象 | 结论 | |
| A | 向装有Fe(NO3)2溶液的试管中加入稀H2SO4后,在试管口观察到红棕色气体 | HNO3分解生成了NO2 |
| B | 向淀粉溶液中加入稀H2SO4,加热几分钟,冷却后再加入新制Cu(OH)2浊液,加热,没有砖红色沉淀生成 | 淀粉没有水解成葡萄糖 |
| C | 向无水乙醇中加入浓H2SO4,加热至170℃产生的气体通入酸性KMnO4溶液,红色褪去 | 使溶液褪色的气体是乙烯 |
| D | 向水玻璃溶液中通入足量CO2 后,产生白色浑浊 | 生成了硅酸沉淀 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝条放人浓硫酸中 | B. | 漂粉精在空气中长期放置 | ||
| C. | 水蒸汽通过Na2O2粉末 | D. | 烧碱在空气中长期放置 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属钠着火时使用泡沫灭火器灭火 | |
| B. | 用试管加热碳酸氢钠固体时使试管口竖直向上 | |
| C. | 蒸馏实验时向蒸馏瓶中放入几粒沸石(或碎瓷片) | |
| D. | 浓硫酸溅到皮肤上时立即用稀氢氧化钠溶液冲洗 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molNa与足量O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子 | |
| B. | 二氧化碳通过Na2O2粉末,反应后固体物质减轻 | |
| C. | 1molNa2O2固体中含离子总数为4NA | |
| D. | 在过氧化钠与水的反应中,每生成0.1mol氧气,转移电子的数目为0.4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
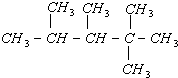 (1)某烯烃,经与氢气加成反应可得到结构简式(如图)的烷烃,则此烯烃可能的结构简式是:CH2=CHCH3CHCH3C(CH3)3、(CH3)2C=CCH3C(CH3)3、(CH3)2CHC=CH2C(CH3)3.
(1)某烯烃,经与氢气加成反应可得到结构简式(如图)的烷烃,则此烯烃可能的结构简式是:CH2=CHCH3CHCH3C(CH3)3、(CH3)2C=CCH3C(CH3)3、(CH3)2CHC=CH2C(CH3)3. ,E是CH3CH3.
,E是CH3CH3.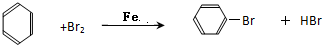 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com