
(14分)下列框图中的字母分别代表一种常见的物质或其溶液,相互之间的转化关系如下图所示(部分产物及反应条件已略去)。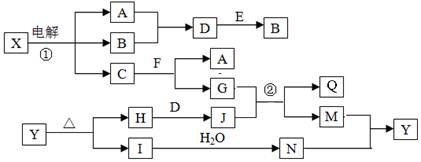
已知A、B为气态单质,F是地壳中含量最多的金属元素的单质:E、H、I为氧化物,E为黑色固体,H为红棕色粉末,I为红棕色气体;M为红褐色沉淀,Q为白色胶状物质。
请回答下列问题:
(1)组成单质F的元素在周期表中的位置是______;C中存在的化学键类型为____;E的化学式是___。
(2)A在B中燃烧的现象是_______ 。
(3) D+E→B的反应中,被氧化与被还原的物质的物质的量之比是_______。
(4)反应①的化学方程式为___________________________________ 。
(5)反应②的离子方程式为___________________________________。
(6)Y受热分解可生成H、I和氧气,.写出该反应的化学方程式:______________________。
(1)第三周期第ⅢA族;离子键、共价键;MnO2 (2)产生苍白色火焰 (3)2:1
(4)2NaCl+2H2O电解2NaOH+H2↑+Cl2↑ (6)3AlO2-+Fe3++6H2O=3Al(OH)3↓+Fe(OH)3↓
(6)4Fe(NO3)3△2Fe2O3+12NO2↑+3O2↑
解析试题分析:F是地壳中含量最多的金属元素的单质,则F为Al;转化关系中X电解得到三种物质,为电解电解质与水型,A、B为气态单质,二者为氢气和氯气,二者反应生成D,D为HCl,E为黑色固体,为氧化物,和HCl反应又生成B气体,A为H2,B为Cl2,E为MnO2,电解X是电解氯化钠溶液,C为NaOH,与Al反应生成A和G,G为NaAlO2;M为红褐色沉淀为Fe(OH)3,所以J是含三价铁离子的物质,是H和D反应生成,证明J为FeCl3,H、I为氧化物判断H为Fe2O3,I为红棕色气体为NO2,结合转化故选可知,N为HNO3,Y为Fe(NO3)3,Q是氢氧化铝,为白色胶状物质。
(1)铝元素于周期表第三周期第ⅢA族。C是氢氧化钠,钠离子与氢氧根之间是离子键,氢氧之间是共价键;E为MnO2。
(2)A为H2,B为Cl2,氢气在氯气燃烧的现象是:气体安静燃烧,火焰呈苍白色,并有白雾产生。(3)D+E→B的反应为MnO2+4HCl(浓)△MnCl2+Cl2↑+2H2O,n(被氧化的物质HCl):n(被还原的物质MnO2)=2:1。
(4)反应①是电解饱和食盐水,反应的的化学方程式为2NaCl+2H2O电解2NaOH+H2↑+Cl2↑。
(5)G(NaAlO2)+J(FeCl3)→M(Fe(OH)3)的反应是在水溶液中发生的双水解反应,反应离子方程式是:3AlO2-+Fe3++6H2O=3Al(OH)3↓+Fe(OH)3↓。
(6)依据分析推断可知Y为Fe(NO3)3,受热分解生成二氧化氮和氧化铁,依据原子守恒配平书写的化学方程式是:4Fe(NO3)3△2Fe2O3+12NO2↑+3O2↑。
考点:考查无机框图题的推断


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案科目:高中化学 来源: 题型:单选题
碳酸钠(Na2CO3)俗称纯碱,是一种重要的基础化工原料,广泛应用于玻璃、造纸等工业。下列与碳酸钠有关的说法正确的是:
| A.Na2CO3的稳定性介于Na2CO3·10H2O和NaHCO3之间 |
| B.“侯氏制碱法”制得的碱是指NaHCO3 |
| C.可用盐酸鉴别Na2CO3和NaHCO3固体 |
| D.纯碱有时可代替烧碱使用,比如溶解石英、促进乙酸乙酯的水解等 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(12分)某研究性学习小组为了测定某品牌合金中铝的含量,现设计了如下实验: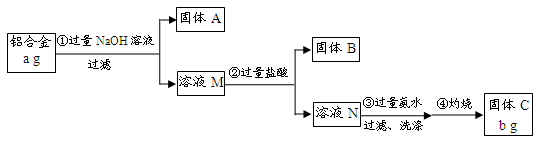
已知:(1)该铝合金的主要成分为铝、镁、铜、硅。
(2)常温下,硅能和NaOH发生反应:Si+2NaOH+H2O===Na2SiO3+2H2↑。
请回答下列问题:
(1)固体A的成分是 ;
(2)生成固体B的离子方程式为 ;
步骤③中生成沉淀的离子方程式为 ;
(3)检验步骤③中沉淀是否洗涤干净的实验操作为
;
(4)该样品中铝的质量分数是 ;(用a、b表示)
(5)下列因操作不当,会使测定结果偏大的是 ;
| A.第①步中加入NaOH溶液不足 | B.第②步中加入盐酸不足时 |
| C.第③步中沉淀未用蒸馏水洗涤 | D.第④步对沉淀灼烧不充分 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(6分)中学化学常见的物质A、B、C、D、E、X有如图所示转化关系。已知A、D是单质,B为氧化物,反应①在高温下发生。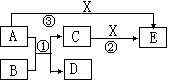
(1)若A、D、X为非金属单质,E是常见的温室气体,则A为____________,X为___________(用化学式填空)。
(2)若A为金属单质,D为非金属单质,X为盐酸,则反应①的化学方程式为________________;反应②的离子方程式________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(10分)如图是部分短周期元素的单质及其化合物(或其溶液)的转化关系,已知B、C、D、E是非金属单质,且在常温常压下都是气体;化合物G的焰色反应为黄色,化合物I和J通常状况下呈气态;反应①是化工生产中的一种重要的固氮反应。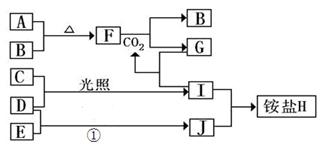
(1)单质E的结构式_____________
(2)F和H2O反应的化学方程式为_____________________________,该反应中被氧化与被还原的物质的物质的量之比是_________________
(3)铵盐H中阳离子的电子式_______________,检验H 中阳离子的方法是____________________
_____________________________________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
碱式硫酸铁[Fe(OH)SO4]是一种用于污水处理的新型高效絮凝剂。工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁的工艺流程如下:
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(18分)铁及其他合物在工业生产中有着广泛的应用。请按要求回答下列问题:
I.工业上利用硫酸铁矿烧渣(主要成分为Fe2O3、Al2O3、SiO2等)为原料提取Fe2O3,工艺流程如下图1:
(1)滤液X中所含金属阳离子有 。
(2)步骤②中理论上发生反应的离子方程式依次为 。
(3)结合图2,分析步骤③调节pH的目的是 。
(4)假设流程中矿渣中的铁元素100%转化到产品中,则硫酸铁矿烧渣样品中Fe2O3的质量分数范围为(含m、n的代数式) 。
(5)请设计实验室中以硫酸铁矿烧渣为原料提取氧化铁的另一种方案:向硫酸铁矿烧渣原料中加入过量稀硫酸、充分搅拌、过滤,再向滤液中加入足量的 溶液,接下来的一系列操作是搅拌、 、洗涤、 ,最后获得纯净的产品Fe2O3。
Ⅱ.几位同学用铁盐溶液清洗试管中银镜,实验设想如下:
(6)甲:认为含Fe3+的盐无法洗去银镜。依据是Fe3+的氧化性(填“强于”或“弱于”) Ag+的氧化性,所以反应Fe3++Ag→Fe2++Ag+不可以发生。
(7)乙:查资料发现,用FeCl3溶液可以清洗银镜,于是他亲自动手实验,发现银镜迅速消失,另外还观察到溶液变为浅绿色;为验证Fe3+的还原产物,可选择的试剂为 。结合甲的分析和自己的实验现象他得出结论:反应Fe2++Ag→Fe3++Ag是(填“可逆”或“不可逆”) 反应。
(8)丙:结合甲、乙的设想,他用Fe(NO3)3溶液做对比实验,发现清洗银镜的速率慢许多,他重新观察乙的实验试管中有白色沉淀,于是结合化学平衡理论分析,得出用FeCl3溶液清洗银镜的离子方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
X、Y、Z、W是元素周期表中原子序数依次增大的四种短周期,其相关信息如下表:
| 元素 | 相关信息 |
| X | X的最高价氧化物对应的水化物化学式为H2XO3 |
| Y | Y是地壳中含量最高的元素 |
| Z | Z的基态原子最外层电子排布式为3s23p1 |
| W | W的一种核素的质量数为28,中子数为14 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
工业上以黄铜矿(主要成分是CuFeS2,杂质不溶于水和酸)为原料,制备蓝色晶体G,其化学式为[Cu(NH3)4]SO4·H2O,涉及流程如下: 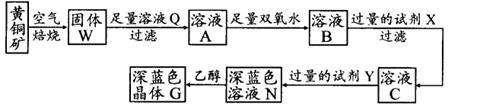
已知25℃时,几种金属氢氧化物的溶度积常数和完全沉淀的pH范围如下表: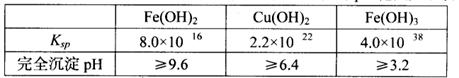
(1)黄铜矿在空气中焙烧能生成铁和铜的低价硫化物,写出其反应的化学方程式: ;
(2)试剂X的化学式为 ;
(3)常温下,0.1 mol/L试剂Y的pH=11,则该温度下,试剂Y的电离常数为 ,用pH试纸测该溶液pH值的方法是 ;
(4)在溶液N中加入乙醇的目的是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com