
 ����ͼ��ʾ�Ǿ��ֻ������ת���ϵ��
����ͼ��ʾ�Ǿ��ֻ������ת���ϵ��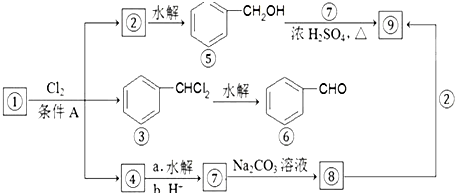
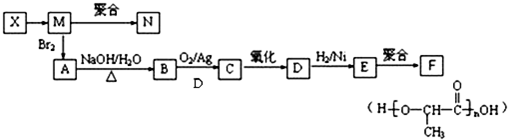
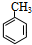 ���ױ��������ڹ��������·������ϵ�ȡ����Ӧ����Ϣݣ����״����Ľṹ��֪��Ϊ
���ױ��������ڹ��������·������ϵ�ȡ����Ӧ����Ϣݣ����״����Ľṹ��֪��Ϊ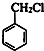 ��������̼�����Ʒ�Ӧ�õ��࣬�ʢߺ����Ȼ������Ϊ
��������̼�����Ʒ�Ӧ�õ��࣬�ʢߺ����Ȼ������Ϊ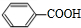 ����Ϊ
����Ϊ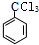 ����Ϊ
����Ϊ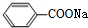 �����״��뱽���ᷴӦ�õ���Ϊ
�����״��뱽���ᷴӦ�õ���Ϊ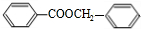 ���ݴ˽��
���ݴ˽�� ���ױ��������ڹ��������·������ϵ�ȡ����Ӧ����Ϣݣ����״����Ľṹ��֪��Ϊ
���ױ��������ڹ��������·������ϵ�ȡ����Ӧ����Ϣݣ����״����Ľṹ��֪��Ϊ ��������̼�����Ʒ�Ӧ�õ��࣬�ʢߺ����Ȼ������Ϊ
��������̼�����Ʒ�Ӧ�õ��࣬�ʢߺ����Ȼ������Ϊ ����Ϊ
����Ϊ ����Ϊ
����Ϊ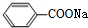 �����״��뱽���ᷴӦ�õ���Ϊ
�����״��뱽���ᷴӦ�õ���Ϊ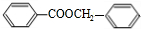 ��
��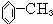 ����������Ӧ���������·���ȡ����Ӧ��
����������Ӧ���������·���ȡ����Ӧ��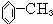 �����գ�
�����գ� ���ɢܡ��ߵ�ˮ��������������������Һ�У�
���ɢܡ��ߵ�ˮ��������������������Һ�У� ������������Һ��
������������Һ��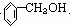 ����Ϊ�����ᣬ���߷����û���Ӧ���ɱ����ᱽ�������ṹʽΪ
����Ϊ�����ᣬ���߷����û���Ӧ���ɱ����ᱽ�������ṹʽΪ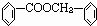 ��
��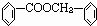 ��
��| Cu/Ag |
| �� |
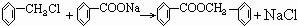 ��
��| Cu/Ag |
| �� |
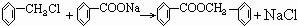 ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ʵ���� | �� | �� | �� | �� |
| ϡ�������/mL | 100 | 200 | 300 | 400 |
| ʣ���������/g | 9.0 | 4.8 | 0 | 0 |
| NO���/L | 1.12 | 2.24 | 3.36 | V |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��H2O��D2O��T2O��Ϊͬλ�� |
| B��pH=1����Һ�У�K+��Na+��NO3-��S2O32-���ܴ������� |
| C��Ԫ�����ڱ��д�������ͬ����Ԫ�ص��⻯����ۡ��е��������� |
| D����Ȳ�����������ֱ���������Ӧ��������������������ͬ�����ɲ�ͬ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��NaHCO3��ˮ�⣺HCO3-+H2O?H3O++CO32- | ||||
| B��1L 0.5mol?L-1ϡ������1L 1mol?L-1����������Һ��Ӧ�ų�57.3kJ��������H2SO4��aq��+2NaOH��aq���TNa2SO4��aq��+2H2O��1������H=-57.3 kJ/mol | ||||
| C������ȼ�ϵ�صĸ�����Ӧʽ��O2+2H2O+4e-�T4OH- | ||||
D���Զ��Ե缫���KCl��Һ��2Cl-+2H2O
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����֪Ceԭ��������58������Ϊ��ϵԪ�� | ||||||||
B�����������ȶ��ĺ�
| ||||||||
| C����Ce��SO4��2��Һ��������������Һ��Ӧ�������ӷ���ʽΪ��Ce4++2Fe2+=Ce3++2Fe3+ | ||||||||
| D�������������Ļ�ѧ����ʽ�ɱ�ʾΪ��Ce+4HI=CeI4+2H2�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com